Thông tin tờ hướng dẫn sử dụng của thuốc Zytiga
Zytiga (Abiraterone) thuộc nhóm thuốc có tên là thuốc ức chế protein kinase. Nhờ ức chế các protein liên quan, Alabrutinib có thể ngăn chặn đường truyền tín hiệu bất thường báo hiệu cho tế bào ung thư nhân lên. Từ đó giúp ngăn chặn sự lây lan của các tế bào ung thư… Dưới đây là nội dung tờ hướng dẫn sử dụng của Thuốc Zytiga (Thông tin bao gồm liều dùng, cách dùng, chỉ định, chống chỉ định, thận trọng, dược lý…):
Nội dung chính
Toggle1. Tên hoạt chất và biệt dược:
Hoạt chất : Abiraterone acetate
Phân loại: Thuốc chống ung thư > Nhóm kháng Androgens.
Nhóm pháp lý: Thuốc kê đơn ETC – (Ethical drugs, prescription drugs, Prescription only medicine)
Mã ATC (Anatomical Therapeutic Chemical): L02BX03.
Biệt dược gốc: Zytiga
Hãng sản xuất : Patheon France (Cơ sở đóng gói, xuất xưởng: Janssen Cilag S.p.A. Italy).
Hãng tiếp thị : Công ty TNHH Johnson & Johnson (Việt Nam).
2. Dạng bào chế – Hàm lượng:
Dạng thuốc và hàm lượng
Viên nén 250 mg.
Viên nén bao phim 500 mg.
Hình ảnh tham khảo:
| ZYTIGA 250MG | ||
| Mỗi viên nén có chứa: | ||
| Abiraterone acetate | …………………………. | 250 mg |
| Tá dược | …………………………. | vừa đủ (Xem mục 6.1) |

3. Thông tin dành cho người sử dụng:
3.1. Zytiga là thuốc gì?
Zytiga có thành phần chính là Abiraterone, là một loại thuốc điều trị ung thư tuyến tiền liệt giai đoạn muộn thông qua tác động vào hormone. Zytiga là biệt dược gốc, hay còn gọi là thuốc phát minh. Zytiga thường được sử dụng cùng với thuốc coritcosteroid (như prednisone hoặc methylprednisolone) để điều trị ung thư tuyến tiền liệt ở nam giới không thể điều trị bằng phẫu thuật hoặc các loại thuốc khác.
3.2. Câu hỏi thường gặp phổ biến:
Cơ chế tác dụng của thuốc Abiraterone như thế nào ?
Ung thư tuyến tiền liệt cần testosterone (Androgen – hormone sinh dục nam) để phát triển. Zytiga (Abiraterone) sẽ ngăn chặn cơ thể bạn tạo ra testosterone (giảm sản xuất androgen trong cơ thể). Điều này có thể giúp làm chậm sự phát triển của bệnh ung thư.
Tại sao Corticosteroid (VD: prednisone) lại được kê đơn cùng với Abiraterone?
Zytiga (Abiraterone) được dùng cùng với prednisone để giúp kiểm soát các tác dụng phụ có thể xảy ra khi điều trị ung thư tuyến tiền liệt. Abiraterone sẽ ngăn chặn việc sản xuất cortisol từ tuyến thượng thận của người bệnh dẫn tới việc thiếu hụt cortisol. Prednisone giúp thay thế lượng cortisol bị mất có thể gây ra các tác dụng phụ như giảm nồng độ kali trong máu, tích nước (phù nề) hoặc gây cao huyết áp.
Zytiga (Abiraterone) có nằm trong danh mục bảo hiểm y tế ở Việt Nam không?
Zytiga có chứa hoạt chất chính là Abiraterone, chất này CÓ nằm trong danh mục bảo hiểm y tế ở Việt Nam, thuốc này chỉ được cấp bảo hiểm ở các bệnh viện hạng II trở lên. Do đó người bệnh có thể được kê đơn và lĩnh thuốc này tại các cơ sở khám chữa bệnh theo tuyến bảo hiểm y tế.
Tôi không thể mua được Zytiga (Abiraterone), hiện tại có thuốc nào có thể mua thay thế được không?
Zytiga là thuốc biệt dược gốc và tính tới năm 2024, có một số biệt dược khác cũng có chứa thành phần Abiraterone giống như Zytiga và được lưu hành tại Việt Nam. Tuy nhiên nếu vẫn không thể tìm được thì có thể báo lại bác sỹ để có thể được tư vấn chuyển đổi sang biệt dược khác để thay thế nếu được đồng ý, không tự ý thay đổi thuốc mà bác sỹ đã chỉ định.
4. Thông tin dành cho nhân viên y tế:
4.1. Chỉ định:
Zytiga dùng kết hợp với prednison hay prednisolon được chỉ định:
Điều trị ung thư tuyến tiền liệt kháng cắt tinh hoàn di căn ở bệnh nhân nam người lớn không triệu chứng hoặc có triệu chứng nhẹ sau thất bại với liệu pháp điều trị triệt tiêu androgen mà chưa được chỉ định hóa trị trên lâm sàng (xem Dược lực học).
Điều trị ung thư tuyến tiền liệt kháng cắt tinh hoàn di căn ở bệnh nhân nam người lớn mà bệnh đang tiến triển trong hoặc sau một đợt hóa trị có chứa docetaxel.
4.2. Liều dùng – Cách dùng:
Cách dùng :
Zytiga phải được dùng ít nhất hai giờ sau khi ăn và không được ăn ít nhất một giờ sau khi uống thuốc. Thuốc phải được uống nguyên viên với nước.
Liều dùng:
Liều khuyến cáo là 1000 mg (4 viên nén 250 mg) liều duy nhất mỗi ngày, không uống cùng thức ăn (xem thông tin về cách dùng). Dùng chung thuốc với thức ăn làm tăng nồng độ abirateron trong cơ thể (xem Tương tác và Dược động học).
Zytiga được dùng với prednison hay prednisolon liều thấp. Liều khuyến cáo của prednison hoặc prednisolon là 10 mg mỗi ngày.
Nên tiếp tục điều trị ức chế chức năng tinh hoàn bằng chất đồng vận LHRH trong thời gian điều trị ở bệnh nhân không phẫu thuật cắt tinh hoàn.
Nên định lượng transaminase trong huyết thanh trước khi bắt đầu điều trị, mỗi hai tuần cho 3 tháng đầu điều trị và mỗi tháng sau đó. Cần kiểm tra huyết áp, kali trong huyết thanh và tình trạng giữ nước định kỳ mỗi tháng. Tuy nhiên, bệnh nhân có nguy cơ cao suy tim sung huyết nên được theo dõi mỗi 2 tuần trong 3 tháng điều trị đầu tiên và sau đó theo dõi hàng tháng (xem phần Cảnh báo).
Ở những bệnh nhân bị hạ kali máu trước đó hoặc những người xuất hiện hạ kali máu trong quá trình điều trị với Zytiga, cân nhắc việc duy trì nồng độ kali của bệnh nhân ở mức ≥ 4,0 mM. Đối với những bệnh nhân xuất hiện độc tính mức độ ≥ 3 bao gồm tăng huyết áp, hạ kali máu, phù nề và các độc tính không phải mineralocorticoid khác, nên ngừng điều trị và tiến hành các biện pháp y khoa thích hợp. Không được tái điều trị với Zytiga cho đến khi các triệu chứng của độc tính đã được giải quyết về mức độ 1 hoặc mức ban đầu.
Trong trường hợp quên liều hàng ngày của Zytiga, prednison hoặc prednisolon, nên tiếp tục điều trị ngày hôm sau với liều hàng ngày thông thường.
Độc tính gan: Nên ngừng điều trị ngay nếu bệnh nhân có xuất hiện tình trạng độc tính gan trong quá trình điều trị (alanin aminotransferase (ALT) hoặc aspartat aminotransferase (AST) tăng > 5 lần giới hạn trên của mức bình thường) (xem Cảnh báo). Sau khi xét nghiệm chức năng gan về giá trị ban đầu của bệnh nhân, có thể tái điều trị với liều giảm còn 500 mg (hai viên) một lần mỗi ngày. Khi bệnh nhân này được tái điều trị, nên theo dõi transaminase huyết thanh ít nhất hai tuần một lần trong 3 tháng và mỗi tháng sau đó. Nếu tái xuất hiện độc tính gan với liều thấp 500 mg mỗi ngày thì nên ngừng điều trị.
Nếu bệnh nhân xuất hiện tình trạng độc tế bào gan nặng (ALT hoặc AST tăng 20 lần giới hạn trên của mức bình thường) vào bất kỳ lúc nào trong thời gian điều trị, nên ngừng điều trị và không nên tái điều trị.
Suy gan:
Không cần điều chỉnh liều cho bệnh nhân suy gan nhẹ trước đó, Child-Pugh loại A.
Nồng độ abirateron trong cơ thể đã được chứng minh tăng lên khoảng 4 lần sau khi uống một liều 1.000 mg abirateron acetat (xem Dược động học) ở những bệnh nhân suy gan trung bình (Child-Pugh loại B). Không có dữ liệu về tính an toàn và hiệu quả lâm sàng của abirateron acetat đa liều khi dùng cho bệnh nhân suy gan trung bình hoặc nặng (Child-Pugh loại B hoặc C). Có thể dự báo không cần điều chỉnh liều. Nên đánh giá thận trọng việc sử dụng Zytiga ở bệnh nhân suy gan trung bình, trong đó lợi ích phải vượt trội rõ ràng so với nguy cơ tiềm ẩn (xem Liều lượng và cách dùng và Dược động học). Không nên sử dụng Zytiga ở bệnh nhân suy gan nặng (xem Chống chỉ định, Cảnh báo và Dược động học).
Suy thận:
Không cần điều chỉnh liều cho bệnh nhân suy thận (xem Dược động học). Tuy nhiên, không có kinh nghiệm lâm sàng ở các bệnh nhân ung thư tuyến tiền liệt và suy thận nặng. Nên thận trọng với các bệnh nhân này (xem Cảnh báo).
Bệnh nhân nhi:
Không dùng thuốc này ở bệnh nhân nhi, vì ung thư tuyến tiền liệt không xuất hiện ở trẻ em và thanh niên.
4.3. Chống chỉ định:
Quá mẫn với hoạt chất hoặc bất kỳ tá dược nào.
Phụ nữ có thai hoặc có khả năng đang mang thai.
Suy gan nặng [Child-Pugh loại C].
4.4 Thận trọng:
Tăng huyết áp, hạ kali máu và giữ nước do thừa mineralocorticoid:
Zytiga có thể gây tăng huyết áp, hạ kali máu và giữ nước (xem Tác dụng ngoại ý) do hậu quả của sự ức chế CYP17 làm tăng nồng độ mineralocorticoid (xem Dược lực học). Sử dụng đồng thời một corticosteroid có tác dụng ức chế tiết hormon adrenocorticotropic (ACTH), dẫn đến làm giảm tỷ lệ và độ nghiêm trọng của các phản ứng bất lợi này. Cần thận trọng khi điều trị các bệnh nhân đang bị bệnh lý y khoa mà có thể bị ảnh hưởng xấu bởi tăng huyết áp, hạ kali máu (như bệnh nhân dùng thuốc glycosid trợ tim) hay giữ nước (như bệnh nhân suy tim), đau thắt ngực nặng hoặc không ổn định, gần đây bị nhồi máu cơ tim hoặc loạn nhịp thất và những người suy thận nặng.
Nên thận trọng sử dụng Zytiga cho bệnh nhân có tiền sử bệnh tim mạch. Các nghiên cứu pha 3 được tiến hành với Zytiga đã loại trừ các bệnh nhân tăng huyết áp không kiểm soát, bệnh tim có biểu hiện lâm sàng nặng như nhồi máu cơ tim hoặc biến cố tắc động mạch trong 6 tháng qua, đau thắt ngực nặng hoặc không ổn định, hoặc suy tim độ III hoặc IV theo phân loại của Hiệp hội tim New York (NYHA) (nghiên cứu 301), hoặc suy tim độ II đến độ IV (nghiên cứu 302) hoặc phân suất tống máu cơ tim < 50%. Trong nghiên cứu 302 bệnh nhân bị rung nhĩ, hoặc chứng loạn nhịp tim khác cần điều trị y khoa đã bị loại trừ. Hiện chưa xác lập được tính an toàn trên bệnh nhân có phân suất tống máu thất trái (LVEF) < 50% hay suy tim độ III hoặc IV theo phân loại của NYHA (trong nghiên cứu 301) hoặc suy tim độ II đến độ IV theo phân loại của NYHA (trong nghiên cứu 302) (xem Tác dụng ngoại ý và Dược lực học).
Trước khi điều trị bệnh nhân có nguy cơ suy tim sung huyết cao (như tiền sử suy tim, tăng huyết áp không kiểm soát, hoặc biến cố tim như bệnh tim do thiếu máu cục bộ), cân nhắc đánh giá chức năng tim (như siêu âm tim). Phải điều trị suy tim và tối ưu hóa chức năng tim trước khi điều trị với Zytiga. Phải điều chỉnh và kiểm soát tăng huyết áp, hạ kali máu và giữ nước. Trong thời gian điều trị, cần phải theo dõi huyết áp, nồng độ kali trong huyết thanh, tình trạng giữ nước (tăng cân, phù ngoại biên), các dấu hiệu và triệu chứng khác của suy tim sung huyết 2 tuần một lần trong 3 tháng, sau đó là hàng tháng và điều chỉnh các bất thường. Quan sát thấy kéo dài khoảng QT ở bệnh nhân bị hạ kali máu có liên quan đến điều trị Zytiga. Đánh giá chức năng tim theo chỉ định lâm sàng, dùng các biện pháp thích hợp, và cân nhắc ngừng điều trị với Zytiga nếu có sự suy giảm chức năng tim đáng kể về mặt lâm sàng (xem Liều lượng và cách dùng).
Độc tính gan và suy gan:
Đã ghi nhận tăng men gan đáng kể dẫn đến ngừng thuốc hoặc điều chỉnh liều trong các nghiên cứu lâm sàng có đối chứng (xem Tác dụng ngoại ý). Nên định lượng transaminase huyết thanh trước khi bắt đầu điều trị, mỗi hai tuần trong ba tháng đầu điều trị và mỗi tháng tiếp theo sau đó. Nên định lượng ngay transaminase huyết thanh nếu có dấu hiệu hoặc triệu chứng gợi ý sự xuất hiện độc tế bào gan. Bất cứ khi nào ALT hay AST tăng cao hơn 5 lần giới hạn trên của mức bình thường phải ngừng điều trị ngay và theo dõi sát chức năng gan. Tái điều trị chỉ khi xét nghiệm chức năng gan trở về mức ban đầu của bệnh nhân và dùng ở mức liều giảm (xem Liều lượng và cách dùng).
Bất kỳ lúc nào trong quá trình điều trị, nếu bệnh nhân bị độc tính gan nặng (ALT hoặc AST cao hơn 20 lần giới hạn trên của mức bình thường) phải ngừng điều trị ngay và không nên tái điều trị.
Bệnh nhân viêm gan vi rút thể hoạt động hoặc có triệu chứng đã được loại ra khỏi các thử nghiệm lâm sàng; do đó, không có dữ liệu hỗ trợ việc sử dụng Zytiga ở đối tượng này.
Không có dữ liệu về tính an toàn và hiệu quả lâm sàng của việc sử dụng abirateron acetat đa liều cho bệnh nhân suy gan mức độ trung bình hoặc nặng (Child-Pugh loại B hoặc C). Việc sử dụng Zytiga cần phải được đánh giá thận trọng ở bệnh nhân suy gan mức độ trung bình, mà trên những bệnh nhân này lợi ích phải vượt trội rõ ràng so với nguy cơ tiềm ẩn (xem Liều lượng và cách dùng và Dược lực học). Không nên sử dụng Zytiga cho bệnh nhân suy gan nặng (xem Liều lượng và cách dùng, Chống chỉ định và Dược lực học).
Ngừng corticosteroid và khắc phục các tình huống stress:
Cần thận trọng và theo dõi tình trạng suy vỏ thượng thận khi bệnh nhân cần ngừng prednison hay prednisolon. Nên theo dõi các triệu chứng tăng mineralocorticoid nếu còn điều trị tiếp tục Zytiga sau khi đã ngừng corticosteroid (xem thông tin ở trên).
Có thể tăng liều corticosteroid trước, trong và sau khi bị các tình huống stress cho các bệnh nhân đang dùng prednison hay prednisolon khi họ phải đối phó với tình trạng stress bất thường này.
Mật độ xương:
Giảm mật độ xương có thể xảy ra ở đàn ông bị ung thư tuyến tiền liệt di căn tiến triển (ung thư tuyến tiền liệt kháng cắt tinh hoàn). Sử dụng Zytiga kết hợp với một glucocorticoid có thể làm tăng tác dụng này.
Sử dụng ketoconazol trước đó:
Tỷ lệ đáp ứng được cho là thấp hơn ở bệnh nhân dùng ketoconazol trước đó để điều trị ung thư tuyến tiền liệt.
Tăng đường huyết:
Sử dụng các glucocorticoid có thể gia tăng nồng độ đường trong máu, do đó nên định lượng đường huyết thường xuyên ở bệnh nhân tiểu đường.
Sử dụng với hóa trị:
Hiện chưa xác lập được tính an toàn và hiệu quả của việc sử dụng đồng thời Zytiga với hóa trị liệu độc tế bào (xem Dược lực học).
Không dung nạp với các tá dược:
Thuốc này có chứa lactose. Những bệnh nhân có các vấn đề di truyền hiếm gặp không dung nạp galactose, thiếu Lapp lactase hoặc kém hấp thụ glucose-galactose không nên dùng thuốc này. Thuốc chứa trên 1 mmol (hay 27,2 mg) natri trong mỗi liều bốn viên. Cân nhắc sử dụng ở các bệnh nhân đang theo chế độ ăn kiêng kiểm soát natri.
Rủi ro tiềm ẩn:
Thiếu máu và rối loạn chức năng tình dục có thể xảy ra ở đàn ông bị ung thư tuyến tiền liệt kháng cắt tinh hoàn di căn, kể cả những người đang được điều trị với Zytiga.
Ảnh hưởng đối với cơ xương:
Các trường hợp bệnh cơ đã được báo cáo ở bệnh nhân được điều trị với Zytiga. Một số bệnh nhân bị tiêu cơ vân cùng với suy thận. Nhiều trường hợp xuất hiện ngay trong tháng điều trị đầu tiên và đã hồi phục sau khi ngừng Zytiga. Nên thận trọng đối với bệnh nhân dùng đồng thời với các loại thuốc đã biết có liên quan đến bệnh cơ/tiêu cơ vân.
Tương tác với các thuốc khác:
Tránh dùng các chất gây cảm ứng mạnh CYP3A4 trong khi điều trị trừ khi không có liệu pháp điều trị thay thế, vì nguy cơ giảm nồng độ abirateron (xem Tương tác).
Tác động của thuốc trên người lái xe và vận hành máy móc.
Abirateron không có hoặc có ảnh hưởng không đáng kể đến khả năng lái xe hoặc vận hành máy móc.
4.5 Sử dụng cho phụ nữ có thai và cho con bú:
Xếp hạng cảnh báo
AU TGA pregnancy category: D
US FDA pregnancy category: NA
Thời kỳ mang thai:
Zytiga không được dùng cho phụ nữ và chống chỉ định cho phụ nữ đang có hoặc có khả năng đang mang thai (xem Chống chỉ định và Anh toàn tiền lâm sàng).
Phụ nữ có khả năng mang thai:
Không có dữ liệu ở người về việc sử dụng Zytiga trong thai kỳ và thuốc này không được sử dụng ở phụ nữ có khả năng mang thai.
Tránh thai ở nam và nữ:
Chưa biết abirateron hoặc các chất chuyển hóa của nó có hiện diện trong tinh dịch hay không. Cần dùng bao cao su nếu bệnh nhân có quan hệ tình dục với phụ nữ đang mang thai. Nếu bệnh nhân có quan hệ tình dục với phụ nữ có khả năng mang thai, cần sử dụng bao cao su cùng với một phương pháp tránh thai hiệu quả khác. Các nghiên cứu ở động vật đã cho thấy độc tính với sinh sản (xem An toàn tiền lâm sàng).
Khả năng sinh sản:
Abirateron có ảnh hưởng đến khả năng sinh sản ở chuột cống đực và chuột cái, nhưng các ảnh hưởng này có thể phục hồi hoàn toàn.
Thời kỳ cho con bú:
Abirateron không được dùng cho phụ nữ.
4.6 Tác dụng không mong muốn (ADR):
Tóm tắt dữ liệu an toàn:
Các phản ứng bất lợi thường gặp nhất là phù ngoại biên, hạ kali máu, tăng huyết áp, nhiễm trùng đường tiết niệu.
Các phản ứng bất lợi quan trọng khác gồm rối loạn tim, nhiễm độc gan, gãy xương và viêm phế nang dị ứng.
Abirateron có thể gây tăng huyết áp, hạ kali máu và giữ nước do hậu quả về dược lực học của cơ chế tác động của thuốc. Trong các nghiên cứu lâm sàng, các phản ứng bất lợi của mineralocorticoid có thể dự đoán trước thường gặp ở bệnh nhân dùng abirateron acetat cao hơn nhóm giả dược: hạ kali máu 21% so với 11%, tăng huyết áp 16% so với 11% và giữ nước (phù ngoại biên) 26% so với 20%. Ở những bệnh nhân điều trị với abirateron acetat, đã quan sát thấy hạ kali máu mức độ 3 và 4 theo CTCAE (phiên bản 3) và tăng huyết áp mức độ 3 và 4 theo CTCAE (phiên bản 3) chiếm tỷ lệ tương ứng là 4% và 2%. Những phản ứng do mineralocorticoid nhìn chung có thể được kiểm soát tốt bằng thuốc. Có thể làm giảm tần suất và mức độ nặng của các phản ứng bất lợi này bằng cách dùng đồng thời với một corticosteroid.
Tóm tắt các phản ứng bất lợi dạng bảng
Trong các nghiên cứu trên bệnh nhân ung thư tuyến tiền liệt tiến triển di căn đang dùng thuốc đồng vận luteinizing hormone-releasing hormone (LHRH) hay đã được cắt bỏ tinh hoàn trước đó, ZYTIGA được dùng với liều 1.000 mg/ngày kết hợp prednison hay prednisolon liều thấp (10 mg/ngày).
Các phản ửng bất lợi quan sát được trong các nghiên cứu lâm sàng và dữ liệu hậu mãi được liệt kê dưới đây theo mức độ tần suất. Các mức độ tần suất được định nghĩa như sau: rất phổ biển (≥ 1/10); phổ biến (≥ 1/100 đến < 1/10); không phổ biến (≥ 1/1.000 đến < 1/100); hiếm (≥ 1/10.000 đến < 1/1.000); rất hiếm (< 1/10.000) và không rõ (không ước lượng được tần suất dựa trên dữ liệu sẵn có).
Trong từng nhóm tần suất, tác dụng ngoại ý được trình bày theo thứ tự mức độ trầm trọng giảm dần.
| Bảng 5. Phản ứng bất lợi được xác định trong các nghiên cứu lâm sàng và dữ liệu hậu mãi | |
| Nhiễm trùng và nhiễm ký sinh trùng | rất phổ biến: nhiễm trùng đường tiết niệu
phổ biến: nhiễm trùng huyết |
| Rối loạn nội tiết | không phổ biến: suy tuyến thượng thận |
| Rối loạn chuyển hóa và dinh dưỡng | rất phổ biến: hạ kali máu
phổ biến: tăng glycerid máu |
| Rối loạn tim | phổ biến: suy tim*, đau thắt ngực, loạn nhịp tim, rung nhĩ, mạch nhanh
không rõ: nhồi máu cơ tim, kéo dài khoảng QT |
| Rối loạn mạch máu | rất phổ biến: tăng huyết áp |
| Rối loạn hô hấp, lồng ngực và trung thất | hiếm: viêm phế nang dị ứnga |
| Rối loạn đường tiêu hóa | rất phổ biến: tiêu chảy
phổ biến: khó tiêu |
| Rối loạn gan mật | phổ biến: tăng alanin aminotransferase, tăng aspartat aminotransferase |
| Rối loạn da và mô dưới da | phổ biến: phát ban |
| Rối loạn cơ xương và mô liên kết | không phổ biến: bệnh cơ, tiêu cơ vân |
| Rối loạn thận và tiết niệu | phổ biến: tiểu máu |
| Rối loạn toàn thân và tình trạng nơi dùng thuốc | rất phổ biến: phù nề ngoại biên |
| Chấn thương, ngộ độc và biến chứng khi điều trị | phổ biến: gãy xương** |
| * Suy tim cũng bao gồm cả suy tim sung huyết, rối loạn chức năng thất trái và phân suất tống máu giảm.
** Gãy xương bao gồm mọl loại gãy trừ gãy xương bệnh lý a Các báo cáo tự phát từ dữ liệu hậu mãi |
|
Cảc phản ứng bất lợi mức độ 3 theo CTCAE (phiên bản 3.0) dưới đây đã xuất hiện ở bệnh nhân được điều trị với abirateron acetat: hạ kali máu 3%; nhiễm trùng đường tiết niệu, tăng alanin aminotransferase, tăng huyết áp, tăng aspartate aminotransferase, gãy xương 2%; phù nề ngoại biên, suy tim, và rung nhĩ, mỗi loại 1%. Tăng glyceride máu mức độ 3 theo CTCAE (phiên bản 3.0) và đau thắt ngực đã xảy ra trên <1% bệnh nhân. Phù nề ngoại biên, hạ kali máu, nhiễm trùng đường tiết niệu, suy tim và gãy xương mức độ 4 theo CTCAE (phiên bản 3.0) xảy ra < 1% bệnh nhân.
Mô tả các phản ứng ngoại ý chọn lọc
Tác động trên tim mạch
Cả 2 nghiên cứu pha 3 không thu nhận các bệnh nhân tăng huyết áp không kiểm soát, bệnh tim nặng trên lâm sàng với bằng chứng của nhồi máu cơ tim, thuyên tắc động mạch trong vòng 6 tháng qua, đau thắt ngực nặng hoặc không ổn định, hay suy tim độ III hoặc IV theo phân loại của NYHA (trong nghiên cứu 301) hoặc suy tim độ II đến độ IV (trong nghiên cứu 302) hoặc giảm phân suất tống máu tim <50%. Tất cả bệnh nhân được thu nhận (cả hai nhóm bệnh nhân dùng thuốc và nhóm dùng giả dược) được điều trị cùng lúc với liệu pháp triệt tiêu androgen, chủ yếu là sử dụng các đồng vận LHRH, mà thường có liên quan với tiểu đường, nhồi máu cơ tim, tai biến mạch máu não và đột tử do tim. Trong các nghiên cứu pha 3, tần suất phản ứng bất lợi tim mạch trong nhóm dùng abirateron acetat so với nhóm dùng giả dược như sau: tăng huyết áp 14,5% so với 10,5%, rung nhĩ 3,4% so với 3,4%, nhịp tim nhanh 2,8% so với 1,7%, cơn đau thắt ngực 1,9% so với 0,9%, suy tim 1,9% so với 0,6% và rối loạn nhịp 1,1% so với 0,4%.
Độc tính gan
Độc tính gan với tăng ALT, aspartat transaminase (AST) và bilirubin toàn phần được báo cáo trên các bệnh nhân điều trị bằng abirateron acetat. Qua tất cả các nghiên cứu lâm sàng, tăng men gan qua xét nghiệm (tăng ALT hay AST > 5 lần giới hạn trên của mức bình thường hoặc tăng bilirubin > 1,5 lần giới hạn trên của mức bình thường) được ghi nhận trong khoảng 4% bệnh nhân dùng abirateron acetat, điển hình trong 3 tháng đầu tiên sau khi bắt đầu điều trị. Trong nghiên cứu lâm sàng 301, các bệnh nhân mà có ALT hay AST ban đầu cao thường dễ tăng chỉ số xét nghiệm chức năng gan hơn bệnh nhân có chỉ số ban đầu bình thường. Nên ngừng điều trị abirateron acetat khi ALT hay AST tăng > 5 lần giới hạn trên của mức bình thường, hoặc bilirubin tăng > 3 lần giới hạn trên của mức bình thường. Có hai trường hợp bệnh nhân được ghi nhận chỉ số chức năng gan tăng cao (xem Cảnh báo và Thận trọng). Hai bệnh nhân này có chỉ số men gan ban đầu bình thường, đã bị ALT hay AST tăng 15 đến 40 lần và bilirubin tăng 2 đến 6 lần giới hạn trên của mức bình thường. Khi ngừng điều trị, chức năng gan của cả hai bệnh nhân đều bình thường trở lại và một bệnh nhân được tái điều trị với ZYTIGA mà không ghi nhận tình trạng tăng lại men gan. Trong nghiên cứu 302, tăng ALT hoặc AST mức độ 3 hoặc 4 đã được quan sát ở 35 (6,5%) bệnh nhân được điều trị với abirateron acetat. Tình trạng tăng aminotransferase được giải quyết ở tất cả các bệnh nhân chỉ trừ 3 bệnh nhân (2 với di căn gan nhiều ổ mới, và 1 với tăng AST khoảng 3 tuần sau liều cuối cùng của abirateron acetat). Ngừng điều trị do tăng ALT và AST lần lượt được báo cáo trong 1,7% và 1,3% số bệnh nhân được điều trị với abirateron acetat và 0,2% và 0% số bệnh nhân được điều trị với giả dược. Không ghi nhận có tử vong do biến cố độc tính gan.
Trong các thử nghiệm lâm sàng, có thể giảm nguy cơ độc tế bào gan bằng cách không thu nhận các bệnh nhân bị viêm gan hoặc có bất thường đáng kể xét nghiệm chức năng gan tại thời điểm ban đầu. Trong thử nghiệm 301 đã loại trừ bệnh nhân có ALT hoặc AST ban đầu > 2,5 lần giới hạn trên của mức bình thường và không di căn gan và > 5 lần giới hạn trên của mức bình thường và có di căn gan. Trong thử nghiệm 302, bệnh nhân có di căn gan là không đủ điều kiện tham gia và đã loại trừ những bệnh nhân có nồng độ ALT và AST ban đầu > 2,5 lần giới hạn trên của mức bình thường. Các bất thường xét nghiệm chức năng gan xuất hiện ở những bệnh nhân tham gia nghiên cứu lâm sàng được theo dõi nghiêm ngặt do đòi hỏi tạm thời ngừng điêu trị và chỉ tái điều trị khi các chỉ số chức năng gan trở về mức ban đầu của bệnh nhân (xem Liều dùng và cách dùng). Bệnh nhân có ALT hay AST tăng > 20 lần giới hạn trên của mức bình thường không được tái điều trị. Tính an toàn khi tái điều trị cho những bệnh nhân như vậy chưa được xác lập. Chưa rõ về cơ chế gây độc tế bào gan của ZYTIGA.
Thông báo cho Bác sĩ những tác dụng không mong muốn gặp phải khi sử dụng thuốc.
4.7 Hướng dẫn cách xử trí ADR:
Ngừng sử dụng thuốc. Với các phản ứng bất lợi nhẹ, thường chỉ cần ngừng thuốc. Trường hợp mẫn cảm nặng hoặc phản ứng dị ứng, cần tiến hành điều trị hỗ trợ (giữ thoáng khí và dùng epinephrin, thở oxygen, dùng kháng histamin, corticoid…).
4.8 Tương tác với các thuốc khác:
Ảnh hưởng của thức ăn đến abirateron acetat:
Sử dụng cùng thức ăn gây tăng đáng kể sự hấp thu abirateron acetat. Chưa xác lập được tính hiệu quả và an toàn khi dùng cùng với thức ăn, vì thế không được uống Abirateron cùng thức ăn.
Tương tác với các thuốc khác:
Khả năng ảnh hưởng của các thuốc khác lên nồng độ abirateron:
Trong một nghiên cứu tương tác dược động học lâm sàng ở người khỏe mạnh được điều trị trước bằng một chất gây cảm ứng mạnh CYP3A4 rifampicin, 600 mg mỗi ngày trong 6 ngày, tiếp nối bởi một liều đơn abirateron acetat 1000 mg, giá trị AUC∞ trung bình trong huyết tương của abirateron giảm 55%.
Tránh sử dụng các chất gây cảm ứng mạnh CYP3A4 (như phenytoin, carbamazepin, rifampicin, rifabutin, rifapentin, phenobarbital, cỏ St John’s [Hypericum perforatum]) trong quá trình điều trị, trừ khi không có liệu pháp điều trị thay thế.
Trong một nghiên cứu tương tác dược động học lâm sàng ở người khỏe mạnh, khi sử dụng đồng thời với ketoconazol là một chất ức chế mạnh CYP3A4, không thấy ảnh hưởng có ý nghĩa lâm sàng trên dược động học của abirateron.
Khả năng ảnh hưởng đến nồng độ của các thuốc khác:
Abirateron là chất ức chế các men chuyển hóa thuốc ở gan, CYP2D6 và CYP2C8.
Trong một nghiên cứu xác định ảnh hưởng của abirateron acetat (phối hợp với prednison) trên liều đơn dextromethorphan cũng là chất nền của CYP2D6, phơi nhiễm toàn thân (AUC) của dextromethorphan tăng khoảng 2,9 lần. Giá trị AUC24 của dextrorphan, một chất chuyển hóa có hoạt tính của dextromethorphan, cũng tăng khoảng 33%.
Nên thận trọng khi sử dụng ZYITGA với các thuốc được chuyển hóa hay hoạt hóa bởi CYP2D6, nhất là các thuốc có chỉ số điều trị hẹp. Nên cân nhắc giảm liều các thuốc có chỉ số điều trị hẹp được chuyển hóa bởi CYP2D6. Các ví dụ về thuốc được chuyển hóa bởi CYP2D6 bao gồm metoprolol, propranolol, desipramin, venlafaxin, haloperidol, risperidon, propafenon, flecainid, codein, oxycodon và tramadol (ba thuốc cuối cùng cần có CYP2D6 để hình thành các chất chuyển hóa có hoạt tính giảm đau).
Trong một thử nghiệm về tương tác thuốc – thuốc với CYP2C8 trên người khỏe mạnh, khi dùng đồng thời pioglitazon với một liều đơn abirateron acetat 1000 mg, giá trị AUC của pioglitazon tăng 46% và AUC của M-III và M-IV, là các chất chuyển hóa còn hoạt tính của pioglitazon, giảm 10% mỗi loại.
Mặc dù các kết quả này cho thấy không có sự gia tăng nồng độ có ý nghĩa lâm sàng khi kết hợp Abirateron với các thuốc được thải trừ chủ yếu qua CYP2C8, bệnh nhân nên được theo dõi các dấu hiệu độc tính liên quan đến chất nền CYP2C8 có chỉ số điều trị hẹp nếu được sử dụng đồng thời với Abirateron.
In vitro, các chất chuyển hóa chính abirateron sulphat và N-oxid abirateron sulphat thể hiện khả năng ức chế chất vận chuyển hấp thu OATP1B1 của gan và do đó có thể tăng nồng độ của thuốc bị thải trừ bởi OATP1B1. Không có dữ liệu lâm sàng để khẳng định tương tác dựa trên chất vận chuyển.
Dùng với các thuốc được biết kéo dài khoảng QT:
Do điều trị với liệu pháp triệt tiêu androgen có thể gây kéo dài khoảng QT, nên thận trọng khi dùng Abirateron với các thuốc được biết kéo dài khoảng QT hoặc các thuốc có khả năng gây xoắn đỉnh như các thuốc chống loạn nhịp tim nhóm IA (ví dụ quinidin, disopyramid) hoặc nhóm III (ví dụ amiodaron, sotalol, dofetilid, ibutilid), methadon, moxifloxacin, các thuốc chống loạn thần.
4.9 Quá liều và xử trí:
Kinh nghiệm về quá liều của Zytiga trên người còn hạn chế.
Không có thuốc giải độc đặc hiệu. Trong trường hợp quá liều, nên ngừng thuốc và điều trị hỗ trợ chung bao gồm theo dõi loạn nhịp tim, hạ kali máu và các dấu hiệu và triệu chứng của giữ nước. Nên đánh giá chức năng gan.
5. Cơ chế tác dụng của thuốc :
5.1. Dược lực học:
Nhóm dược lý điều trị: điều trị nội tiết, chất đối kháng hormon và các chất khác liên quan, mã ATC: L02BX03.
Zytiga làm giảm lượng testosteron và các androgen khác trong huyết thanh xuống mức thấp hơn so với khi dùng đồng vận LHRH đơn thuần hoặc phẫu thuật cắt tinh hoàn. Tác dụng này do sự ức chế chọn lọc men CYP17 cần thiết cho sinh tổng hợp androgen. Kháng nguyên đặc hiệu tiền liệt tuyến (Prostate specific antigen – PSA) là dấu ấn sinh học ở các bệnh nhân ung thư tuyến tiền liệt. Trong một nghiên cứu lâm sàng pha 3 ở bệnh nhân đã thất bại với hóa trị với taxan trước đó, 38% bệnh nhân được điều trị bằng abirateron acetat được ghi nhận giảm ít nhất 50% so với mức PSA ban đầu so với 10% bệnh nhân được điều trị bằng giả dược.
Cơ chế tác dụng:
Trên in vivo, abirateron acetat (Zytiga) được chuyển hóa thành abirateron, một chất ức chế sinh tổng hợp androgen. Cụ thể, abirateron ức chế chọn lọc men 17α-hydroxylase/C17,20-lyase (CYP17). Men này được bộc lộ trong và cần thiết cho quá trình sinh tổng hợp androgen ở tinh hoàn, tuyến thượng thận và khối u mô tiền liệt tuyến. CYP17 xúc tác quá trình chuyển đổi pregnenolon và progesteron thành các tiền chất của testosteron, DHEA và androstenedion, tương ứng, bằng việc hydroxyl hóa vị trí 17α và chia cắt nối C17,20. Ức chế CYP17 cũng dẫn đến tăng sản xuất mineralocorticoid tại tuyến thượng thận.
Các phương pháp điều trị làm giảm nồng độ androgen sẽ có hiệu quả trên ung thư tiền liệt tuyến nhạy cảm với androgen. Các biện pháp điều trị triệt tiêu androgen như điều trị với các đồng vận LHRH hay cắt tinh hoàn, làm giảm tạo ra androgen từ tinh hoàn nhưng không ảnh hưởng đến sự tạo thành androgen tại tuyến thượng thận hay khối u. Điều trị với Abirateron làm giảm nồng độ testosteron huyết thanh xuống đến mức không phát hiện được (bằng các định lượng thương mại) khi điều trị kết hợp với đồng vận LHRH (hay phẫu thuật cắt tinh hoàn).
[XEM TẠI ĐÂY]
5.2. Dược động học:
Dược động học của abirateron và abirateron acetat sau khi uống abirateron acetat được nghiên cứu trên những người khỏe mạnh, các bệnh nhân ung thư tiền liệt tuyến tiến triển di căn và những người không bị ung thư có suy chức năng gan hoặc thận. Abirateron acetat được chuyển hóa nhanh chóng trong cơ thể (in vivo) thành abirateron, một chất có tác dụng ức chế sinh tổng hợp androgen (xem Đặc tính dược lực học)
Hấp thu:
Sau khi uống abirateron acetat lúc đói, abirateron đạt nồng độ tối đa trong huyết thanh sau gần 2 giờ.
Uống abirateron acetat cùng với thức ăn làm gia tăng nồng độ trung bình abirateron trong cơ thể đến 10 lần (AUC) và 17 lần (Cmax) so với lúc đói, tùy thuộc vào lượng mỡ có trong thức ăn. Do thay đổi tính chất và thành phần thức ăn nên uống Abirateron trong bữa ăn có khả năng dẫn đến nhiều nồng độ thuốc cao khác nhau. Vì vậy không được dùng Abirateron với thức ăn. Nên uống thuốc ít nhất hai giờ sau khi ăn và không được ăn ít nhất một giờ sau uống thuốc. Nên nuốt nguyên viên thuốc với nước.
Phân bố:
Khả năng gắn kết với protein trong huyết thanh người của 14C-abirateron lên tới 99,8%. Thể tích phân bố biểu kiến gần 5630 L, cho thấy abirateron phân bố rộng rãi đến các tổ chức mô ngoại biên.
Chuyển hóa sinh học:
Sau khi uống 14C-abirateron acetat dạng viên nang, abirateron acetat được thủy phân thành abirateron. Chất này được tiếp tục chuyển hóa qua các phản ứng sulfat hóa, hydroxyl hóa và oxid hóa chủ yếu tại gan. Đa số hoạt chất đánh dấu phóng xạ lưu hành trong máu (gần 92%) được thấy dưới dạng các chất chuyển hóa của abirateron. Trong 15 chất chuyển hóa phát hiện được có 2 chất chính là abirateron sulphat và N-oxid abirateron sulphat, mỗi chất chiếm khoảng 43% tổng hoạt độ phóng xạ.
Thải trừ:
Ở người khỏe mạnh, thời gian bán thải trung bình của abirateron trong huyết thanh là 15 giờ. Sau khi uống 14C-abirateron acetat 1.000 mg, gần 88% liều có hoạt tính phóng xạ được thấy trong phân và khoảng 5% trong nước tiểu. Chất thải chính hiện diện trong phân là abirateron acetat dạng chưa chuyển hóa (55% của liều uống) và abirateron (22% của liều uống).
Bệnh nhân suy gan:
Dược động học của abirateron được nghiên cứu trên nhóm bệnh nhân suy gan nhẹ và trung bình tồn tại trước đó (xếp loại Child-Pugh A và B) và trên nhóm người chứng khỏe mạnh bình thường. Sau khi uống liều đơn 1.000 mg, ở các bệnh nhân đang bị suy gan nhẹ và trung bình, nồng độ abirateron trong cơ thể đã gia tăng khoảng từ 11% (các bệnh nhân suy gan nhẹ) và 260% (các bệnh nhân suy gan trung bình). Thời gian bán thải trung bình của abirateron kéo dài đến khoảng 18 giờ ở các bệnh nhân suy gan nhẹ và khoảng 19 giờ trên các bệnh nhân suy gan trung bình.
Trong một thử nghiệm khác, dược động học của abirateron được đánh giá ở các đối tượng đang suy gan nặng (n=8) (Child-Pugh loại C) và 8 đối tượng đối chứng khỏe mạnh với chức năng gan bình thường. Phơi nhiễm toàn thân (AUC) với abirateron đã tăng khoảng 600% và tỷ lệ thuốc tự do tăng 80% ở các đối tượng suy gan nặng so với các đối tượng có chức năng gan bình thường.
Không cần thiết phải chỉnh liều cho các bệnh nhân suy gan nhẹ trước đó. Thận trọng khi sử dụng abirateron acetat ở các bệnh nhân bị suy gan trung bình, là những người mà lợi ích phải vượt trội rõ ràng so với rủi ro tiềm ẩn. Không nên dùng abirateron acetat cho bệnh nhân suy gan nặng. Đối với các bệnh nhân có xuất hiện độc tính tế bào gan trong khi dùng Abirateron có thể phải tạm ngừng điều trị và cần chỉnh liều.
Bệnh nhân suy thận:
Dược động học của abirateron tương tự giữa nhóm bệnh nhân bệnh thận giai đoạn cuối phải lọc thận định kỳ và nhóm người đối chứng khỏe mạnh có chức năng thận bình thường. Không ghi nhận có sự tăng nồng độ abirateron sau uống liều đơn 1.000 mg ở nhóm bệnh nhân bệnh thận giai đoạn cuối đang lọc thận định kỳ.
Không cần giảm liều dùng Zytiga trên các bệnh nhân suy thận kể cả suy thận nặng. Tuy nhiên, không có kinh nghiệm lâm sàng trên bệnh nhân ung thư tuyến tiền liệt và suy thận nặng. Thận trọng khi sử dụng ở các bệnh nhân này.
5.3. Hiệu quả lâm sàng:
Hiệu quả của Zytiga được xác lập qua hai nghiên cứu lâm sàng pha 3 đa trung tâm, ngẫu nhiên, có đối chứng với giả dược (nghiên cứu 301 và 302) trên các bệnh nhân ung thư tiền liệt tuyến kháng cắt tinh hoàn di căn.
Nghiên cứu 302 thu nhận các bệnh nhân chưa dùng docetaxel, trong khi nghiên cứu 301 thu nhận các bệnh nhân đã được dùng docetaxel trước đó. Các bệnh nhân đang dùng đồng vận LHRH hoặc đã được cắt tinh hoàn bằng phẫu thuật trước đó. Ở nhóm bệnh nhân dùng thuốc Zytiga liều 1.000 mg/ngày kết hợp với prednison hay prednisolon liều thấp 5 mg hai lần mỗi ngày. Nhóm bệnh nhân đối chứng dùng giả dược kết hợp với prednison hoặc prednisolon liều thấp 5 mg hai lần mỗi ngày.
Những thay đổi về nồng độ PSA trong huyết thanh một cách độc lập thường không phải lúc nào cũng dự đoán được lợi ích lâm sàng. Vì thế, bệnh nhân trong cả hai nghiên cứu được khuyến cáo duy trì việc điều trị nghiên cứu cho đến khi tiêu chí ngưng thuốc được đáp ứng theo quy định cụ thể dưới đây cho mỗi nghiên cứu.
Không được dùng spironolacton trong cả hai nghiên cứu vì spironolacton gắn với thụ thể androgen và có thể làm tăng nồng độ PSA.
Nghiên cứu 302 (bệnh nhân chưa được hóa trị):
Nghiên cứu này tuyển chọn các bệnh nhân chưa được hóa trị mà không có triệu chứng hoặc có triệu chứng nhẹ và hóa trị chưa được chỉ định lâm sàng. Cơn đau nhất trong 24 giờ có điểm số từ 0 đến 1 dựa trên Chỉ số đánh giá đau – Biểu mẫu vắn tắt (Brief Pain Inventory-Short Form, BPI-SF) được xem là không có triệu chứng, và điểm số 2-3 được xem là có triệu chứng nhẹ.
Trong nghiên cứu 302, (n = 1088) tuổi trung bình của bệnh nhân được tuyển chọn là 71 tuổi ở bệnh nhân dùng Zytiga cùng với prednison hoặc prednisolon và là 70 tuổi ở các bệnh nhân dùng giả dược cùng với prednison hoặc prednisolon. Số lượng bệnh nhân điều trị với Zytiga theo chủng tộc là 520 người da trắng (95,4%), 15 người da đen (2,8%), 4 người châu Á (0,7%) và 6 người chủng tộc khác (1,1%). Theo thang điểm thể trạng ECOG, 76% bệnh nhân có điểm 0, và 24% bệnh nhân có điểm 1 trên cả hai nhóm. 50% bệnh nhân chỉ bị di căn xương, thêm 31% bệnh nhân di căn xương và mô mềm hoặc hạch bạch huyết và 19% bệnh nhân chỉ bị di căn mô mềm hoặc hạch bạch huyết. Các bệnh nhân có di căn nội tạng bị loại trừ khỏi nghiên cứu. Các tiêu chí hiệu quả phối hợp chính là sống còn toàn bộ và sống không bệnh tiến triển trên X quang (rPFS). Ngoài việc đo lường các tiêu chí phối hợp chính, lợi ích cũng được đánh giá dựa trên thời gian cho đến khi sử dụng thuốc opioid để giảm đau do ung thư, thời gian đến khi bắt đầu hóa trị liệu độc tế bào, thời gian đến khi suy giảm hoạt động cơ thể theo thang điểm ECOG với ≥1 điểm và thời gian đến khi có tiến triển về PSA được dựa trên tiêu chuẩn Nhóm làm việc Ung thư Tuyến tiền liệt-2 (PCWG2).
Các điều trị trong nghiên cứu được ngừng tại thời điểm có tiến triển lâm sàng rõ ràng. Điều trị cũng có thể được ngừng tại thời điểm có tiến triển trên X quang được xác nhận theo quyết định của nghiên cứu viên.
Sống không bệnh tiến triển trên X quang được đánh giá dựa trên việc sử dụng các nghiên cứu hình ảnh tuần tự theo quy định của tiêu chuẩn PCWG2 (đối với các tổn thương xương) và tiêu chuẩn đánh giá đáp ứng trên khối u (RECIST) được điều chỉnh (đối với tổn thương mô mềm).
Việc phân tích rPFS đã sử dụng đánh giá tiến triển trên X quang được xem xét toàn bộ.
Tại thời điểm phân tích rPFS theo kế hoạch đã có 401 biến cố, trong đó 150 (28%) bệnh nhân được điều trị với Zytiga và 251 (46%) bệnh nhân được điều trị với giả dược có bằng chứng của sự tiến triển trên X quang hoặc tử vong. Có sự khác biệt đáng kể về rPFS giữa các nhóm điều trị (xem Bảng 1 và Hình 1).
Bảng 1: Nghiên cứu 302: sống không bệnh tiến triển trên X quang của các bệnh nhân được điều trị hoặc với ZYTIGA hoặc với giả dược kết hợp với prednison hoặc prednisolon cộng với các thuốc đồng vận LHRH hay cắt tinh hoàn trước đó
| . | ZYTIGA
(N=546) |
Giả dược
(N=542) |
| Sống không bệnh tiến triển trên X quang (rPFS) | ||
| Tiến triển hoặc tử vong | 150 (28%) | 251 (46%) |
| Trung vị rPFS theo tháng (95% CI) | Không đạt được
(11,66, NE) |
8,3
(8,12, 8,54) |
| Giá trị p* | < 0.0001 | |
| Tỉ số nguy hại** (95% CI) | 0,425 (0,347, 0,522) | |
| NE= Not Estimated: không ước tính được
* Giá trị p được lấy từ một phân tích log-rank được phân tầng theo thang điểm ECOG ban đầu (0 hoặc 1) ** Tỉ số nguy hại <1 ưu thế cho ZYTIGA |
||
Hình 1 – Đường cong Kaplan Meier về sống còn không tiến triển bệnh trên X quang của các bệnh nhân được điều trị hoặc với ZYTIGA hoặc với giả dược kết hợp với prednison hoặc prednisolon cộng với các thuốc đồng vận LHRH hay cắt tinh hoàn bằng phẫu thuật trước đó
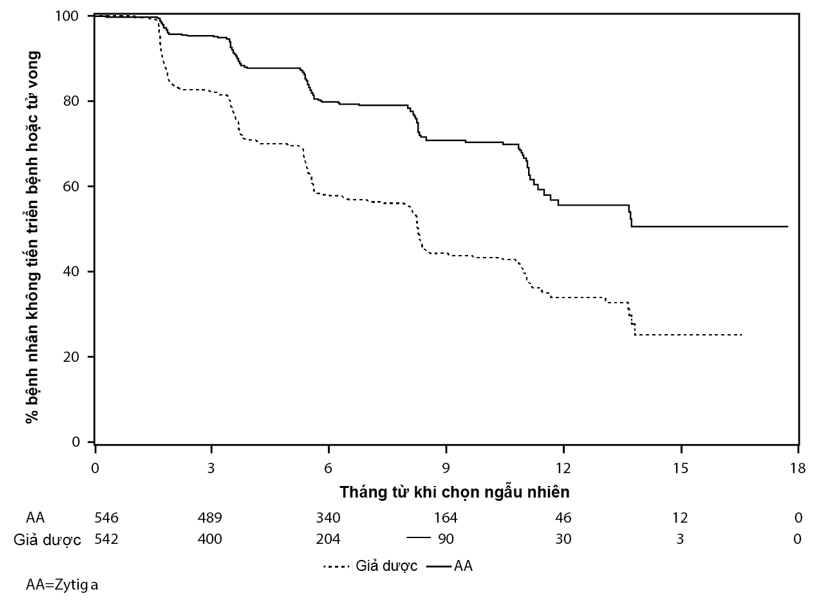
Tuy nhiên, dữ liệu về đối tượng tiếp tục được thu thập đến ngày phân tích tạm thời thứ hai về tỉ lệ sống còn toàn bộ (OS). Kết quả xem xét hình ảnh X quang của rPFS được nghiên cứu viên tiến hành dưới dạng phân tích theo dõi độ nhạy được trình bày trong Bảng 2 và Hình 2. 607 đối tượng có tiến triển trên X quang hoặc tử vong: 271 (50%) trong nhóm abirateron acetat và 336 (62%) trong nhóm giả dược. Điều trị với abirateron acetat giảm nguy cơ tiến triển trên X quang hoặc tử vong 47% so với giả dược (HR=0,530; 95% CI: [0,451; 0,623]; p < 0,0001). Trung vị rPFS là 16,5 tháng ở nhóm abirateron acetat và 8,3 tháng ở nhóm giả dược.
Bảng 2: Nghiên cứu 302: sống còn không tiến triển bệnh trên X quang của bệnh nhân hoặc điều trị với ZYTIGA hoặc giả dược kết hợp với prednison hoặc prednisolon cùng với chất đồng vận LHRH hoặc phẫu thuật cắt tinh hoàn trước đó (vào thời điểm phân tích giữa kỳ lần hai của nghiên cứu viên xem xét OS)
| . | ZYTIGA
(N=546) |
Giả dược
(N=542) |
| Sống không bệnh tiến triển trên X quang (rPFS) | ||
| Tiến triển hoặc tử vong | 271 (50%) | 336 (62%) |
| Trung vị rPFS theo tháng (95% CI) | 16,5 (13,80, 16,79) | 8,3 (8,05, 9,43) |
| Giá trị p* | < 0.0001 | |
| Tỉ số nguy hại** (95% CI) | 0,530 (0,451, 0,623) | |
| NE= Not Estimated: không ước tính được
* Giá trị p được lấy từ một phân tích log-rank được phân tầng theo thang điểm ECOG ban đầu (0 hoặc 1) ** Tỉ số nguy hại <1 ưu thế cho ZYTIGA |
||
Hình 2- Đường cong Kaplan Meier về sống còn không tiến triển bệnh trên X quang của các bệnh nhân hoặc điều trị với ZYTIGA hoặc giả dược kết hợp với prednison hoặc prednisolon cộng với các thuốc đồng vận LHRH hay phẫu thuật cắt tinh hoàn trước đó (vào thời điểm phân tích giữa kỳ lần hai của nghiên cửu viên xem xét OS)

Sau khi ghi nhận 333 trường hợp tử vong đã tiến hành một phân tích theo kế hoạch về sống còn toàn bộ. Nghiên cứu được mở mù dựa trên tầm quan trọng của lợi ích lâm sàng quan sát được và bệnh nhân trong nhóm giả dược được đề nghị cho điều trị với Zytiga. Sống còn toàn bộ dài hơn ở nhóm Zytiga so với giả dược với nguy cơ tử vong giảm 25% (Tỉ số nguy hại = 0,752; 95% CI: [0,606 – 0,934], p=0,0097), nhưng sống còn toàn bộ không đạt và kết quả tạm thời không đạt giới hạn ngừng đã định trước (pre-specified stopping boundary) về ý nghĩa thống kê (xem Bảng 3). Tiếp tục theo dõi sống còn sau phân tích giữa kỳ này.
Sau khi ghi nhận 741 trường hợp tử vong (trung vị theo dõi lên đến 49 tháng) đã tiến hành phân tích cuối cùng theo kế hoạch về sống còn toàn bộ. 65% (354 trên 546) bệnh nhân điều trị với Zytiga, so với 71% (387 trên 542) bệnh nhân điều trị với giả dược, đã tử vong. Sống còn toàn bộ có ý nghĩa thống kê ưu thế cho nhóm điều trị với Zytiga được chứng minh qua tỷ lệ giảm 19,4% nguy cơ tử vong (Tỉ số nguy hại = 0,806; 95% CI: [0,697 ; 0,931], p=0,0033) và sự cải thiện trung vị sống còn toàn bộ 4,4 tháng (Zytiga 34,7 tháng, giả dược 30,3 tháng) (xem Bảng 3 và Hình 3). Sự cải thiện này được chứng minh mặc dù 44% bệnh nhân trong nhóm giả dược đã dùng Zytiga như liệu pháp tiếp theo.
Bảng 3: Nghiên cứu 302: Sống còn toàn bộ của bệnh nhân được điều trị hoặc với ZYTIGA hoặc với giả dược kết họp với prednison hoặc prednisolon cộng với các chất đồng vận LHRH hay cắt tinh hoàn bằng phẫu thuật trước đó
| . | ZYTIGA
(N=546) |
Giả dược
(N=542) |
|
| Phân tích sống còn giữa kỳ | |||
| Tử vong (%) | 147 (27%) | 186 (34%) | |
| Trung vị thời gian sống còn (tháng) (95% CI) | Không đạt được (không ước tính được, không ước tính được) | 27,2 (25,95, không ước tính được) | |
| Giá trị p* | 0,0097 | ||
| Tỉ số nguy hại** (95% CI) | 0,752 (0,606; 0,934) | ||
| Phân tích sống còn cuối cùng | |||
| Tử vong (%) | 354 (65%) | 387 (71%) | |
| Trung vị thời gian sống còn toàn bộ theo tháng (95% CI) | 34,7 (32,7; 36,8) | 30,3 (28,7; 33,3) | |
| Giá trị p* | 0,0033 | ||
| Tỉ số nguy hại** (95% CI) | 0,806 (0,697; 0,931) | ||
| * Giá trị p được lấy từ một phân tích log-rank được phân tầng theo thang điểm ECOG ban đầu (0 hoặc 1)
** Tỉ số nguy hại <1 ưu thế cho ZYTIGA |
|||
Hình 3 – Đường cong Kaplan Meier về sống còn trên bệnh nhân được điều tri hoặc với ZYTIGA hoặc với giả dược kết hợp với prednison hoặc prednisolon cộng với các chất đồng vận LHRH hay cắt tinh hoàn bằng phẫu thuật trước đó, phân tích cuối cùng
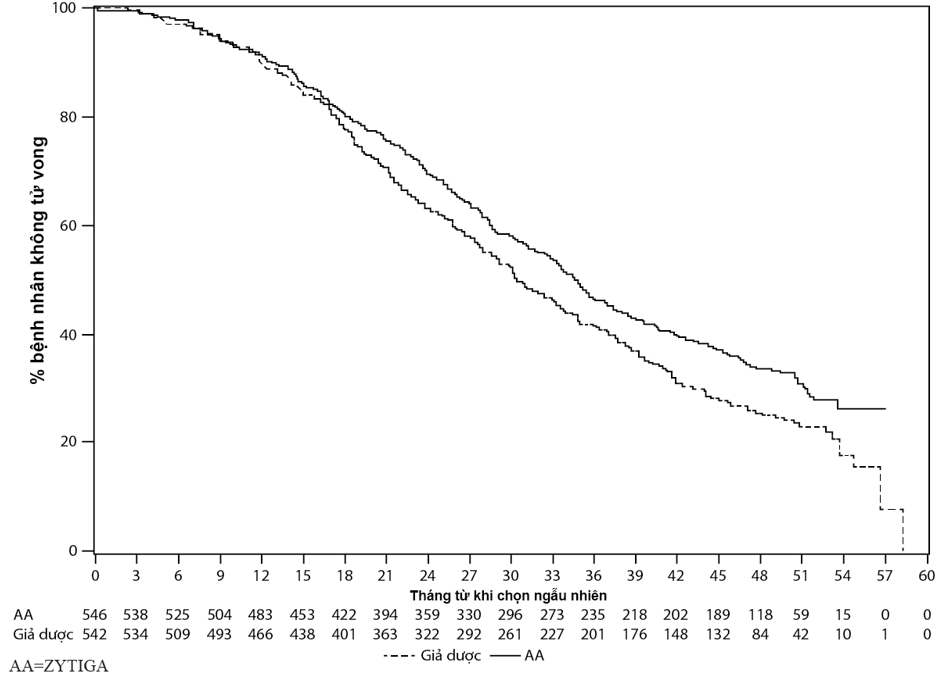
Bên cạnh sự cải thiện về sống còn toàn bộ và rPFS quan sát được, lợi ích của việc điều trị với Zytiga so với giả dược đã được chứng minh trên tất cả các đánh giá về tiêu chí phụ như sau:
-Thời gian cho đến khi có tiến triển về PSA dựa trên tiêu chuẩn PCWG2: Trung vị thời gian cho đến khi tiến triển về PSA là 11,1 tháng đối với bệnh nhân được điều trị với Zytiga và 5,6 tháng đối với bệnh nhân dùng giả dược (HR = 0,488, 95% CI: [0,420, 0,568], p < 0,0001). Thời gian cho đến khi tiến triển về PSA dài hơn gần gấp đôi với bệnh nhân điều trị Zytiga (HR = 0,488). Tỷ lệ các bệnh nhân có đáp ứng về PSA được xác nhận là cao hơn ở nhóm điều trị Zytiga so với nhóm giả dược (62% so với 24%, p < 0,0001). Ở các đối tượng có tổn thương mô mềm có thể đánh giá, đã thấy có sự gia tăng đáng kể số lượng đáp ứng khối u hoàn toàn và một phần khi được điều trị với Zytiga.
-Thời gian đến khi sử dụng thuốc opioid để giảm đau do ung thư: Trung vị thời gian đến khi sử dụng thuốc opioid để giảm đau do ung thư tuyến tiền liệt tại thời điểm phân tích cuối cùng là 33,4 tháng trên những bệnh nhân điều trị Zytiga và với bệnh nhân dùng giả dược là 23,4 tháng (HR = 0,721; 95% CI: [0,614, 0,846], p = 0,0001).
-Thời gian cho đến khi bắt đầu hóa trị liệu độc tế bào: Trung vị thời gian cho đến khi bắt đầu hóa trị liệu độc tế bào là 25,2 tháng đối với bệnh nhân điều trị Zytiga và 16,8 tháng cho các bệnh nhân dùng giả dược (HR = 0,580, 95% CI: [0,487, 0,691], p < 0,0001).
Thời gian cho đến khi suy giảm hoạt động cơ thể theo thang điểm ECOG với ≥ 1 điểm: Trung vị thời gian cho đến khi suy giảm hoạt động cơ thể theo thang điểm ECOG với điểm ≥ 1 là 12,3 tháng đối với bệnh nhân điều trị Zytiga và 10,9 tháng đối với bệnh nhân dùng giả dược (HR = 0,821, 95% CI: [0,714, 0,943], p = 0,0053).
-Các tiêu chí nghiên cứu sau đây đã chứng minh lợi thế có ý nghĩa thống kê thuận lợi cho việc điều trị với Zytiga:
Đáp ứng mục tiêu: đáp ứng mục tiêu được định nghĩa là tỷ lệ các bệnh nhân với bệnh có thể đo lường được đạt được đáp ứng hoàn toàn hoặc một phần theo tiêu chuẩn RECIST (kích thước nốt bạch huyết ban đầu phải ≥ 2cm được xem là tổn thương đích). Tỷ lệ các bệnh nhân với bệnh có thể đo lường được vào thời điểm ban đầu đã có đáp ứng mục tiêu là 36% trong nhóm điều trị Zytiga và 16% ở nhóm giả dược (p < 0,0001).
Đau: Điều trị bằng Zytiga làm giảm đáng kể nguy cơ tiến triển mức độ đau trung bình 18% so với giả dược (p = 0,0490). Trung vị thời gian cho đến khi có tiến triển là 26,7 tháng ở nhóm điều trị Zytiga và 18,4 tháng ở nhóm giả dược.
Thời gian dẫn đến suy giảm sức khỏe theo thang điểm FACT-P (Tổng điểm) (đánh giá tình trạng sức khỏe của bệnh nhân ung thư tuyến tiền liệt): Điều trị bằng Zytiga giảm nguy cơ suy giảm sức khỏe theo thang điểm FACT-P (Tổng điểm) 22% so với giả dược (p = 0,0028). Trung vị thời gian đến khi suy giảm sức khỏe theo thang điểm FACT-P (Tổng điểm) là 12,7 tháng ở nhóm điều trị Zytiga và 8,3 tháng ở nhóm giả dược.
Nghiên cứu 301 (bệnh nhân đã nhận được hóa trị liệu trước đó):
Nghiên cứu 301 lựa chọn các bệnh nhân đã được điều trị trước đó với docetaxel. Các bệnh nhân không cần phải có tiến triển bệnh với docetaxel, vì độc tính của liệu pháp hóa trị này có thể dẫn đến ngừng điều trị.
Bệnh nhân được duy trì với điều trị của nghiên cứu đến khi có tiến triển về PSA (được xác nhận là tăng 25% so với mức ban đầu hoặc mức gần triệt tiêu (nadir) của bệnh nhân) cùng với tiến triển trên X quang được xác định trong đề cương nghiên cứu và tiến triển về triệu chứng hoặc lâm sàng. Bệnh nhân trước đó được điều trị ung thư tuyến tiền liệt với ketoconazol bị loại ra khỏi nghiên cứu này. Tiêu chí hiệu quả chính là sống còn toàn bộ.
Trung vị tuổi của bệnh nhân được chọn là 69 (khoảng 39 đến 95). Số bệnh nhân được điều trị với Zytiga theo nhóm chủng tộc gồm 737 người da trắng (93,2%), 28 người da đen (3,5%), 11 người châu Á (1,4%) và 14 nhóm khác (1,8%). 11% bệnh nhân tham gia nghiên cứu 301 có điểm 2 theo thang điểm ECOG ; 70% có bằng chứng bệnh tiến triển trên X quang với có hoặc không có sự tiến triển PSA; 70% đã nhận được một hóa trị liệu độc tế bào trước đó và 30% nhận được hai hóa trị liệu độc tế bào trước đó. 11% bệnh nhân được điều trị với Zytiga có hiện diện của di căn gan.
Trong một phân tích theo dự định đã được tiến hành sau khi quan sát thấy 552 trường hợp tử vong, 42% (333 trong 797) bệnh nhân được điều trị Zytiga đã tử vong so với 55% (219 trong 398) bệnh nhân nhóm chứng. Nhóm bệnh nhân điều trị Zytiga có sự cải thiện đáng kể có ý nghĩa thống kê về trung vị thời gian sống còn toàn bộ. (xem Bảng 4).
Bảng 4: Thời gian sống còn toàn bộ của các bệnh nhân được điều trị hoặc với ZYTIGA hoặc với giả dược kết hợp với prednison/ prednisolon cộng với thuốc đồng vận LHRH hoặc cắt tinh hoàn bằng phẫu thuật trước đó
| ZYTIGA
(N=797) |
GIẢ DƯỢC
(N=398) |
|
| Phân tích sống còn ban đầu | ||
| Tử vong (%) | 333 (42%) | 219 (55%) |
| Trung vị thời gian sống còn (tháng) (95% CI) | 14,8 (14,1,15,4) | 10,9 (10,2, 12,0) |
| Giá trị pa | <0,0001 | |
| Tỉ số nguy hạib (95% CI) | 0,646 (0,543, 0,768) | |
| Phân tích sống còn cập nhật | ||
| Tử vong (%) | 501 (63%) | 274 (69%) |
| Trung vị thời gian sống còn (tháng) (95% CI) | 15,8 (14,8, 17,0) | 11,2 (10,4, 13,1) |
| Tỉ số nguy hạib (95% CI) | 0,740 (0,638, 0,859) | |
| a Giá trị p được lấy từ một phân tích log-rank được phân tầng theo thang điểm ECOG (0-1 so với 2), điểm đau (không có so với có), số đợt hóa trị liệu trước đó (1 so với 2), và loại tiến triển bệnh (chỉ có PSA so với theo X quang).
b Tỉ số nguy hại được lấy từ một mô hình nguy hại phân tầng tỷ lệ. Tỉ số nguy hại < 1 ưu thế cho ZYTIGA |
||
Vào tất cả các thời điểm đánh giá sau khởi sự điều trị vài tháng, bệnh nhân điều trị với Zytiga luôn có tỉ lệ sống còn cao hơn nhóm đối chứng (xem Hình 4).
Hình 4- Đường biểu diễn Kaplan Meier về sống còn của các bệnh nhân điều trị hoặc với ZYTIGA hoặc với giả dược kết hợp với prednison hoặc prednisolon cộng với thuốc đồng vận LHRH hoặc cắt tinh hoàn bằng phẫu thuật trước đó
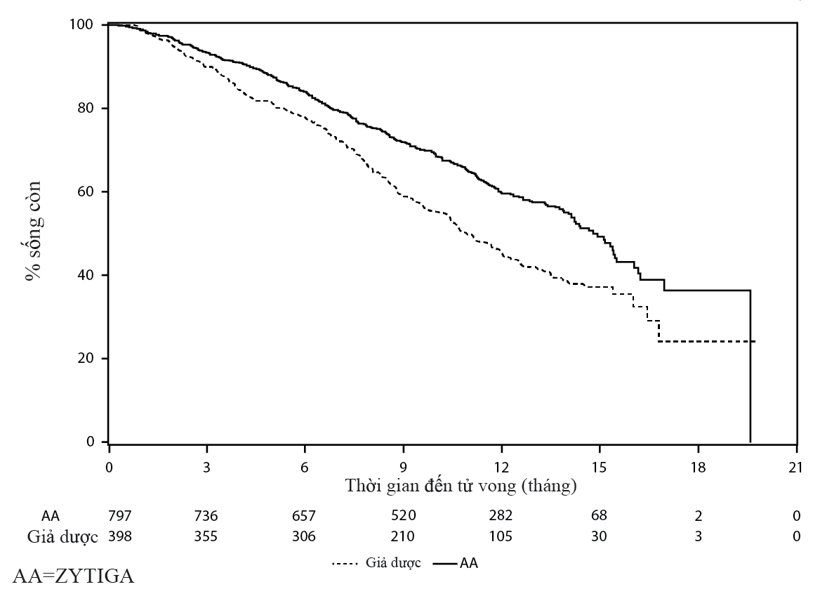
Phân tích sống còn theo phân nhóm đã cho thấy lợi ích sống còn nhất quán ở nhóm điều trị với Zytiga (xem Hình 5).
Hình 5: sống còn toàn bộ theo các phân nhóm: tỉ số nguy hại (Hazard Ratio) và khoảng tin cậy 95%
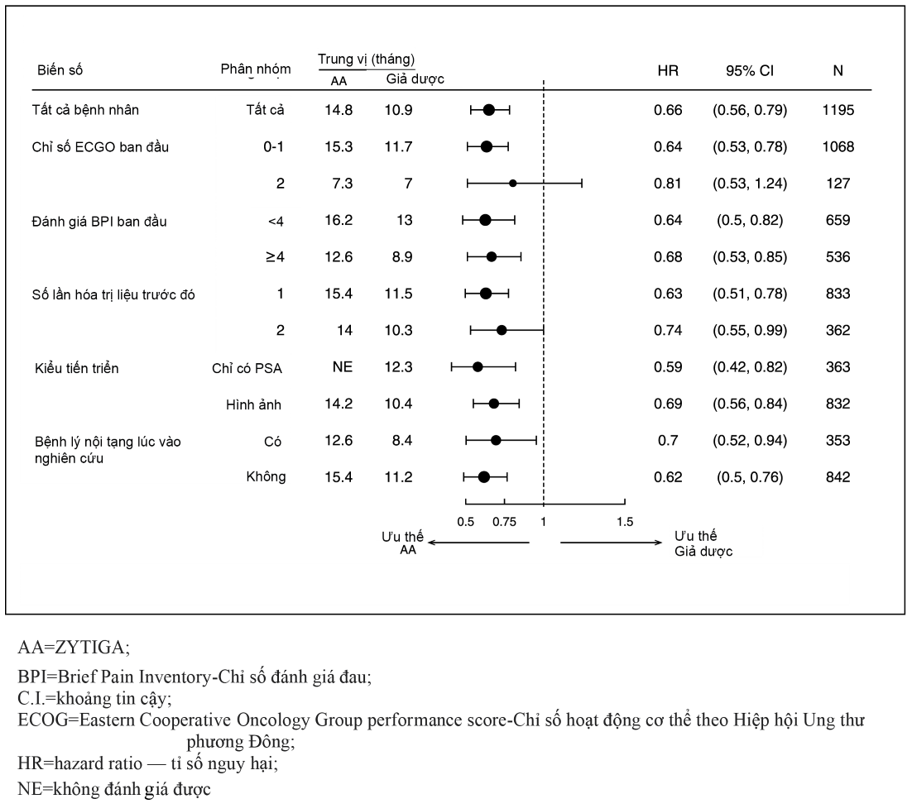
Bên cạnh sự cải thiện thời gian sống còn toàn bộ, Zytiga còn chứng tỏ sự ưu thế có ý nghĩa thống kê trên các tiêu chí nghiên cứu phụ sau khi hiệu chỉnh cho đa phương pháp phân tích như sau:
Bệnh nhân dùng Zytiga có tỉ lệ đáp ứng PSA toàn bộ (được định nghĩa là giảm hơn ≥ 50% so với trị số ban đầu) cao hơn đáng kể so với nhóm đối chứng: 38% so với 10%, p < 0,0001.
Trung vị thời gian đến khi tiến triển về PSA là 10,2 tháng ở bệnh nhân dùng Zytiga so với 6,6 tháng ở nhóm đối chứng (HR= 0,580; 95% CI: [0,462, 0,728], p < 0,0001).
Trung vị thời gian sống còn không có bệnh tiến triển trên X-quang là 5,6 tháng ở bệnh nhân dùng Zytiga so với 3,6 tháng ở bệnh nhân dùng giả dược (HR= 0,673; 95% CI: [0,585, 0,776], p < 0,0001).
Đau:
Tỉ lệ bệnh nhân được giảm đau thuộc nhóm Zytiga cao hơn nhóm chứng có ý nghĩa thống kê (44% so với 27%, p = 0,0002). Bệnh nhân được xem có đáp ứng giảm đau khi chỉ số đánh giá mức độ đau tồi tệ nhất BPI-SF giảm ít nhất 30% so với ban đầu trong 24 giờ qua mà không có tăng chỉ số dùng thuốc giảm đau được ghi nhận qua hai lần đánh giá liên tiếp cách nhau 4 tuần. Phân tích đánh giá đáp ứng giảm đau chỉ bao gồm các bệnh nhân có chỉ số đau ban đầu ≥ 4 và ít nhất có được một chỉ số đau sau đánh giá lúc ban đầu (n=512).
Bệnh nhân điều trị Zytiga có tỉ lệ tiến triển đau thấp hơn nhóm giả dược vào các thời điểm 6 tháng (22% so với 28%), 12 tháng (30% so với 38%) và 18 tháng (35% so với 46%). Tiến triển đau được định nghĩa là tình trạng tăng chỉ số đánh giá mức độ đau tồi tệ nhất theo BPI-SF ≥ 30% so với ban đầu trong 24 giờ qua mà không có giảm chỉ số dùng thuốc giảm đau được ghi nhận qua hai lần đánh giá liên tiếp, hay sự gia tăng chỉ số dùng thuốc giảm đau ≥ 30% được ghi nhận qua hai lần đánh giá liên tiếp. Thời gian cho tới khi tiến triển đau tại mốc thứ 25% (25th percentile) là 7,4 tháng của nhóm Zytiga so với 4,7 tháng của nhóm giả dược.
Biến cố liên quan đến xương:
Tỉ lệ biến cố liên quan xương được ghi nhận thấp hơn ở nhóm Zytiga so với nhóm giả dược tại các thời điểm 6 tháng (18% so với 28%), 12 tháng (30% so với 40%), và 18 tháng (35% so với 40%). Thời gian cho tới khi xuất hiện biến cố liên quan đến xương tại mốc 25% (25thpercentile) của nhóm Zytiga dài gấp đôi nhóm giả dược: 9,9 tháng so với 4,9 tháng. Biến cố liên quan đến xương được định nghĩa bao gồm: gãy xương bệnh lý, chèn ép tủy sống, xạ trị giảm nhẹ triệu chứng ở xương, hoặc phẫu thuật xương.
5.4. Dữ liệu tiền lâm sàng:
Trong tất cả các nghiên cứu độc tính trên động vật, nồng độ testosterone tuần hoàn đã giảm đáng kể. Kết quả đã quan sát thấy sự giảm khối lượng các cơ quan và những thay đổi hình thái học và/hoặc mô bệnh học tại các cơ quan sinh sản, và tuyến thượng thận, tuyến yên và tuyến vú. Các thay đổi này có khả năng phục hồi hoàn toàn hay một phần. Những thay đổi ở cơ quan sinh sản và các cơ quan nhạy cảm với androgen là nhất quán với tác dụng dược lý của abirateron. Tất cả các thay đổi nội tiết liên quan đến điều trị đã phục hồi như cũ hoặc được giải quyết sau khoảng thời gian hồi phục 4 tuần.
Trong các nghiên cứu khả năng sinh sản trên chuột cống cái và chuột cống đực, abirateron acetat làm giảm khả năng sinh sản, tuy nhiên khả năng sinh sản phục hồi hoàn toàn trong vòng 4 đến 16 tuần sau khi ngừng abirateron acetat.
Trong một nghiên cứu phát triển độc tính trên chuột, abirateron acetat ảnh hưởng lên quá trình mang thai bao gồm cả giảm trọng lượng của thai nhi và giảm sự sống còn. Ảnh hưởng trên cơ quan sinh dục ngoài đã được quan sát thấy mặc dù abirateron acetat không gây quái thai. Trong các nghiên cứu về khả năng sinh sản và phát triển độc tính trên chuột này, tất cả các ảnh hưởng đều liên quan đến tác dụng dược lý của abirateron.
Ngoài những thay đổi của cơ quan sinh sản quan sát được trong tất cả các nghiên cứu độc tính trên động vật, dữ liệu tiền lâm sàng cho thấy không có nguy cơ đặc biệt đối với con người, dựa trên các nghiên cứu quy ước về an toàn dược lý, độc tính liều lặp lại và độc tính gen. Abirateron acetat không phải là chất gây ung thư trong một nghiên cứu trong 6 tháng ở chuột chuyển gen (Tg.rasH2). Trong một nghiên cứu 24 tháng về khả năng gây ung thư ở chuột cống, abirateron acetat làm tăng tỷ lệ mắc khối u tế bào kẽ ở tinh hoàn. Phát hiện này được xem là liên quan đến tác dụng dược lý của abirateron và đặc hiệu trên chuột. Abirateron acetat không phải là chất gây ung thư ở chuột cống cái.
*Lưu ý:
Các thông tin về thuốc trên Pharmog.com chỉ mang tính chất tham khảo – Khi dùng thuốc cần tuyệt đối tuân theo theo hướng dẫn của Bác sĩ
Chúng tôi không chịu trách nhiệm về bất cứ hậu quả nào xảy ra do tự ý dùng thuốc dựa theo các thông tin trên Pharmog.com
6. Phần thông tin kèm theo của thuốc:
6.1. Danh mục tá dược:
Tá dược viên nén: colloidal silicon dioxid, natri croscarmellose, lactose monohydrat, magnesi stearat, cellulose vi tinh thể, povidon, natri lauryl sulfat.
6.2. Tương kỵ :
Do không có các nghiên cứu về tính tương kỵ của thuốc, không trộn lẫn thuốc này với các thuốc khác.
6.3. Bảo quản:
Không bảo quản ở nhiệt độ trên 30°C.
Không để thuốc tiếp xúc với ánh nắng mặt trời.
6.4. Thông tin khác :
Mô tả:
Viên nén 250mg: Viên nén hình bầu dục, màu trắng đến trắng ngà, khắc chữ AA250 trên một mặt.
6.5 Tài liệu tham khảo:
HDSD Thuốc Zytiga do Công ty Janssen Cilag sản xuất (2017).
7. Người đăng tải /Tác giả:
Bài viết được sưu tầm hoặc viết bởi: Bác sĩ nhi khoa – Đỗ Mỹ Linh.
Kiểm duyệt , hiệu đính và đăng tải: PHARMOG TEAM


