Thuốc INVEGA SUSTENNA là thuốc gì ? Dưới đây là nội dung tờ hướng dẫn sử dụng gốc của Thuốc INVEGA SUSTENNA (Thông tin bao gồm liều dùng, cách dùng, chỉ định, chống chỉ định, thận trọng, dược lý…)
Nội dung chính
Toggle1. Tên hoạt chất và biệt dược:
Hoạt chất : Paliperidone
Phân loại: Thuốc chống loạn thần.
Nhóm pháp lý: Thuốc kê đơn ETC – (Ethical drugs, prescription drugs, Prescription only medicine)
Mã ATC (Anatomical Therapeutic Chemical): N05AX13.
Brand name: INVEGA SUSTENNA.
Hãng sản xuất : Janssen Pharmaceutica N.V.
2. Dạng bào chế – Hàm lượng:
Dạng thuốc và hàm lượng
Hỗn dịch tiêm giải phóng kéo dài: hộp 1 bơm tiêm đóng sẵn (tương ứng các thể tích 0,25 mL/ 0,5 mL/ 0,75 mL/ 1 mL/ 1,5 mL) với pít-tông và nắp chụp kim bằng cao su bromobutyl, nút hãm tự động, 1 kim tiêm an toàn cỡ 22 dài 3,8 cm (1½-inch) và 1 kim tiêm an toàn cỡ 23 dài 2,5 cm (1-inch).
Mỗi 0,25 mL/ 0,5 mL/ 0,75 mL/ 1 mL/ 1,5 mL: Paliperidon 25 mg, 50 mg, 75 mg, 100 mg hoặc 150 mg.
Hỗn dịch màu trắng đến trắng ngà.
Thuốc tham khảo:
| INVEGA SUSTENNA 100mg | ||
| Mỗi ml hỗn dịch tiêm có chứa: | ||
| Paliperidone | …………………………. | 100 mg |
| Tá dược | …………………………. | vừa đủ (Xem mục 6.1) |

| INVEGA SUSTENNA 150mg | ||
| Mỗi 1.5ml hỗn dịch tiêm có chứa: | ||
| Paliperidone | …………………………. | 150 mg |
| Tá dược | …………………………. | vừa đủ (Xem mục 6.1) |

3. Video by Pharmog:
[VIDEO DƯỢC LÝ]
————————————————
► Kịch Bản: PharmogTeam
► Youtube: https://www.youtube.com/c/pharmog
► Facebook: https://www.facebook.com/pharmog/
► Group : Hội những người mê dược lý
► Instagram : https://www.instagram.com/pharmogvn/
► Website: pharmog.com
4. Ứng dụng lâm sàng:
4.1. Chỉ định:
INVEGA SUSTENNA được chỉ định trong điều trị tâm thần phân liệt và phòng ngừa tái phát triệu chứng tâm thần phân liệt cho bệnh nhân người lớn (từ 18 tuổi trở lên).
4.2. Liều dùng – Cách dùng:
Cách dùng :
Hướng dẫn sử dụng
– xem Hình 3.


Cách dùng
INVEGA SUSTENNA chỉ được dùng để tiêm trong cơ. Tiêm chậm và sâu vào trong cơ. Cần thận trọng tránh tiêm nhầm vào mạch máu. Việc tiêm thuốc cho bệnh nhân nên được thực hiện bởi các nhân viên y tế. Chỉ tiêm một lần, không chia liều thành nhiều lần tiêm. Không tiêm tĩnh mạch hoặc tiêm dưới da.
Kích thước của kim tiêm INVEGA SUSTENNA vào cơ delta được quyết định dựa theo cân nặng của bệnh nhân. Với bệnh nhân nặng ≥ 90 kg (≥ 200 lb), nên dùng kim tiêm 1½ inch, cỡ 22. Với bệnh nhân nặng < 90 kg (< 200 lb), nên dùng kim tiêm 1 inch, cỡ 23. Nên tiêm luân phiên vào cơ delta ở cả hai bên.
Kích thước khuyến cáo của kim tiêm INVEGA SUSTENNA vào cơ mông là 1½-inch, cỡ 22. Nên tiêm vào vùng một phần tư trên – ngoài vùng mông. Nên tiêm luân phiên vào cơ mông ở hai bên.
Do paliperidon là chất chuyển hóa có hoạt tính chính của risperidone nên cần thận trọng khi dùng INVEGA SUSTENNA cùng với risperidon hoặc paliperidon đường uống trong khoảng thời gian kéo dài. Có ít dữ liệu an toàn liên quan đến sử dụng đồng thời INVEGA SUSTENNA với các thuốc chống loạn thần khác.
Với những bệnh nhân chưa dùng paliperidon đường uống hoặc risperidon đường uống hoặc đường tiêm bao giờ, nên bắt đầu với paliperidon đường uống hoặc risperidon đường uống để tạo khả năng dung nạp trước khi dùng INVEGA SUSTENNA.
Liều dùng:
Liều khởi đầu khuyến cáo của INVEGA SUSTENNA là 150 mg paliperidon trong ngày thứ nhất, và 100 mg paliperidon một tuần sau đó, tiêm cơ delta. Liều duy trì hàng tháng khuyến cáo là 75 mg paliperidon; một số bệnh nhân có thể dùng liều thấp hơn hoặc cao hơn trong khoảng khuyến cáo từ 25 đến 150 mg paliperidon, tùy thuộc vào khả năng dung nạp và/hoặc hiệu quả của thuốc trên từng bệnh nhân. Sau liều khởi đầu thứ 2, có thể dùng liều duy trì hàng tháng, tiêm cơ delta hoặc cơ mông.
Liều duy trì có thể được điều chỉnh hàng tháng. Cần xem xét đặc tính giải phóng kéo dài của INVEGA SUSTENNA khi chỉnh liều (xem Dược động học) do hiệu quả đầy đủ của liều điều chỉnh có thể không rõ ràng trong vài tháng.
Quên liều
Tránh quên liều
Nên dùng INVEGA SUSTENNA liều khởi đầu thứ 2 sau liều thứ nhất một tuần. Để tránh quên liều, có thể cho bệnh nhân dùng liều thứ 2 trước hoặc sau thời điểm 1 tuần khoảng 2 ngày. Tương tự, liều thứ 3 và các liều tiếp theo sau liều giai đoạn điều trị khởi đầu được khuyến cáo nên tiêm hàng tháng. Để tránh quên liều hàng tháng, có thể cho bệnh nhân tiêm thuốc trong vòng 7 ngày trước hoặc sau thời điểm hàng tháng này.
Nếu ngày dự định cho lần tiêm INVEGA SUSTENNA thứ hai (1 tuần ± 2 ngày) bị quên, nên lặp lại liều khởi đầu tùy thuộc vào khoảng thời gian tính từ lần tiêm đầu tiên của bệnh nhân.
Quên tiêm liều thứ 2 (< 4 tuần kể từ lần tiêm đầu tiên)
Nếu thời gian quên ít hơn 4 tuần kể từ lần tiêm đầu tiên, nên tiêm lần thứ 2 ngay cho bệnh nhân với liều 100 mg paliperidon vào cơ delta trong thời gian sớm nhất có thể. Nên tiêm INVEGA SUSTENNA lần thứ 3 với liều 75 mg paliperidon vào cơ delta hoặc cơ mông 5 tuần sau lần tiêm đầu tiên (bất kể lần thứ hai tiêm vào thời điểm nào). Sau đó, cần thực hiện chu kỳ tiêm thuốc hàng tháng vào cơ delta hoặc cơ mông với liều từ 25 đến 150 mg paliperidon tùy thuộc vào khả năng dung nạp và/hoặc hiệu quả trên từng bệnh nhân.
Quên liều khởi đầu thứ 2 (4-7 tuần kể từ lần tiêm đầu tiên)
Nếu thời gian quên 4-7 tuần kể từ lần tiêm đầu tiên, bắt đầu lại liều bằng 2 lần tiêm 100 mg paliperidon thuốc theo thứ tự sau: tiêm càng sớm càng tốt vào cơ delta, sau đó 1 tuần lại tiêm vào cơ delta, tiếp theo duy trì chu kỳ tiêm thuốc hàng tháng vào cơ delta hoặc cơ mông với liều từ 25 đến 150 mg paliperidon tùy thuộc vào khả năng dung nạp và hiệu quả trên từng bệnh nhân.
Quên liều khởi đầu thứ 2 (>7 tuần kể từ lần tiêm đầu tiên)
Nếu thời gian quên nhiều hơn 7 tuần kể từ lần tiêm đầu tiên, nên bắt đầu lại quy trình tiêm INVEGA SUSTENNA từ liều khởi đầu như khuyến cáo ở trên.
Quên liều duy trì (từ 1 tháng đến 6 tuần)
Sau 2 liều khởi đầu, nên tiêm INVEGA SUSTENNA hàng tháng. Nếu thời gian quên ít hơn 6 tuần kể từ lần tiêm trước, cần tiêm ngay càng sớm càng tốt một liều ổn định như các liều trước đó, sau đó tiếp tục tiêm thuốc theo chu kỳ hàng tháng.
Quên liều duy trì (> 6 tuần đến 6 tháng)
Nếu quên hơn 6 tuần kể từ lần tiêm trước, nên thực hiện theo các bước sau:
Đối với bệnh nhân ở trạng thái ổn định khi dùng liều 25 đến 100 mg paliperidon
Tiêm ngay càng sớm càng tốt vào cơ delta liều đã giúp bệnh nhân ổn định trước đó.
Tiêm cùng liều đó vào cơ delta 1 tuần sau (ngày 8).
Lặp lại chu kỳ tiêm thuốc hàng tháng vào cơ delta hoặc cơ mông liều trong khoảng 25 mg đến 150 mg paliperidon tùy theo khả năng dung nạp của bệnh nhân và/hoặc hiệu quả của thuốc.
Đối với bệnh nhân ở trạng thái ổn định khi dùng liều 150 mg paliperidon
Tiêm ngay càng sớm càng tốt vào cơ delta liều 100 mg paliperidon.
Tiêm cùng liều 100 mg paliperidon vào cơ delta 1 tuần sau (ngày 8).
Lặp lại chu kỳ tiêm thuốc hàng tháng vào cơ delta hoặc cơ mông liều từ 25 mg đến 150 mg paliperidon tùy theo khả năng dung nạp của bệnh nhân và/hoặc hiệu quả của thuốc.
Quên liều duy trì (> 6 tháng)
Nếu quên hơn 6 tháng kể từ lần tiêm trước đó, nên bắt đầu lại quy trình tiêm INVEGA SUSTENNA từ mũi tiêm khởi đầu như đã khuyến cáo ở trên.
Đối tượng đặc biệt
Trẻ em (dưới 18 tuổi)
Chưa có nghiên cứu về tính an toàn và hiệu quả của INVEGA SUSTENNA ở bệnh nhân < 18 tuổi.
Người cao tuổi (từ 65 tuổi trở lên)
Nói chung, liều INVEGA SUSTENNA khuyến cáo cho bệnh nhân cao tuổi có chức năng thận bình thường giống với liều khuyến cáo cho bệnh nhân trưởng thành trẻ tuổi có chức năng thận bình thường. Do người cao tuổi có thể bị suy giảm chức năng thận, xem mục Suy thận để chỉnh liều cho bệnh nhân suy thận.
Suy thận
INVEGA SUSTENNA chưa được nghiên cứu một cách hệ thống ở các bệnh nhân suy thận (xem Dược động học). Với bệnh nhân suy thận nhẹ (độ thanh thải creatinin ≥ 50 và < 80 mL/phút), liều INVEGA SUSTENNA khởi đầu khuyến cáo là tiêm cơ delta liều 100 mg paliperidon vào ngày thứ nhất và liều 75 mg paliperidon sau đó một tuần. Sau đó, tiếp tục tiêm cơ delta hoặc cơ mông hàng tháng với liều 50 mg paliperidon vào cơ delta hoặc cơ mông, thay đổi liều trong khoảng 25 đến 100 mg tùy thuộc vào khả năng dung nạp của bệnh nhân và/hoặc hiệu quả của thuốc.
Không nên dùng INVEGA SUSTENNA cho bệnh nhân suy thận trung bình hoặc nặng (độ thanh thải creatinin < 50 mL/phút).
Suy gan
INVEGA SUSTENNA chưa được nghiên cứu ở bệnh nhân suy gan. Theo một nghiên cứu với paliperidon đường uống, không cần điều chỉnh liều với bệnh nhân bị suy gan nhẹ hoặc trung bình. Paliperidon chưa được nghiên cứu trên bệnh nhân suy gan nặng (xem Dược động học).
Đối tượng khác
Không cần điều chỉnh liều INVEGA SUSTENNA theo giới tính, sắc tộc hay đối tượng hút thuốc lá (với phụ nữ có thai và cho con bú, xem Sử dụng ở phụ nữ có thai và cho con bú).
Chuyển từ một thuốc chống loạn thần khác
Chưa có dữ liệu thu được một cách có hệ thống nào đề cập đến việc chuyển từ một thuốc chống loạn thần khác sang INVEGA SUSTENNA ở bệnh nhân tâm thần phân liệt hay việc dùng đồng thời INVEGA SUSTENNA với các thuốc chống loạn thần khác. Với những bệnh nhân chưa từng dùng paliperidon đường uống hoặc risperidon đường uống hoặc đường tiêm, khuyến cáo nên dùng paliperidon đường uống hoặc risperidon đường uống để tạo khả năng dung nạp trước khi bắt đầu dùng INVEGA SUSTENNA (xem Liều lượng và Cách dùng).
Có thể từ từ ngừng dùng các thuốc chống loạn thần đường uống khác khi bắt đầu điều trị với INVEGA SUSTENNA. Cần khởi đầu điều trị với INVEGA SUSTENNA như đã nêu trong phần đầu của mục Liều lượng và Cách dùng.
Khi chuyển thuốc cho bệnh nhân đang ở trạng thái ổn định với một thuốc chống loạn thần tác dụng kéo dài đường tiêm khác, cần bắt đầu liệu trình điều trị với INVEGA SUSTENNA thay cho lần tiêm tiếp theo của thuốc đó. Sau đó tiếp tục dùng INVEGA SUSTENNA hàng tháng. Không cần thực hiện liều khởi đầu 1 tuần như mô tả ở phần đầu của mục Liều lượng và Cách dùng.
Bệnh nhân đã đạt trạng thái ổn định với các liều khác nhau của RISPERDAL CONSTA hỗn dịch tiêm bắp giải phóng kéo dài có thể đạt một nửa sự phơi nhiễm ở trạng thái ổn định có hoạt tính tương đương khi duy trì điều trị hàng tháng với các liều INVEGA SUSTENNA như sau:
– xem Bảng 1.

Việc ngừng sử dụng thuốc chống loạn thần trước đó cần được xem xét cho phù hợp với thông tin kê toa. Cần cân nhắc tới đặc tính giải phóng kéo dài của thuốc khi ngừng sử dụng INVEGA SUSTENNA. Cũng như khuyến cáo với các thuốc chống loạn thần khác, nên đánh giá định kỳ sự cần thiết của việc tiếp tục sử dụng các thuốc điều trị triệu chứng ngoại tháp.
4.3. Chống chỉ định:
INVEGA SUSTENNA chống chỉ định cho những bệnh nhân có tiền sử quá mẫn với paliperidon hoặc bất cứ thành phần nào của thuốc. Do paliperidon là một chất chuyển hóa có hoạt tính của risperidon nên chống chỉ định dùng INVEGA SUSTENNA trên những bệnh nhân có tiền sử quá mẫn với risperidon.
4.4 Thận trọng:
Hội chứng thần kinh ác tính do thuốc hướng thần
Hội chứng thần kinh ác tính do thuốc hướng thần (NMS) được biểu hiện bằng thân nhiệt tăng, cứng cơ, rối loạn thần kinh thực vật, rối loạn ý thức và tăng nồng độ creatin phosphokinase huyết thanh đã được báo cáo xảy ra khi sử dụng thuốc chống loạn thần, kể cả paliperidon. Triệu chứng lâm sàng khác có thể bao gồm tiểu myoglobin (tiêu cơ vân) và suy thận cấp. Nếu bệnh nhân có biểu hiện các triệu chứng và dấu hiệu chỉ điểm của NMS thì phải ngừng sử dụng thuốc chống loạn thần, kể cả INVEGA SUSTENNA.
Loạn động muộn
Thuốc có đặc tính đối vận thụ thể dopamin gây nên loạn động muộn được biểu hiện bằng các vận động không tự chủ và có tính chất nhịp, rõ rệt nhất ở lưỡi và/hoặc mặt. Nếu các dấu hiệu và triệu chứng của loạn động muộn xuất hiện thì phải cân nhắc ngừng sử dụng các thuốc chống loạn thần, kể cả INVEGA SUSTENNA.
Khoảng QT
Cũng như với thuốc chống loạn thần khác, cần thận trọng khi sử dụng INVEGA SUSTENNA cho bệnh nhân có tiền sử rối loạn nhịp tim, bệnh nhân có hội chứng QT dài bẩm sinh và khi sử dụng đồng thời với những thuốc đã được biết gây kéo dài khoảng QT (xem Dược lực học – Ảnh hưởng lên khoảng QT/QTc và sinh lý điện tim).
Phản ứng quá mẫn
Mặc dù cần xác định khả năng dung nạp paliperidon hoặc risperidon đường uống trước khi bắt đầu điều trị INVEGA SUSTENNA, nhưng trong quá trình theo dõi hậu mãi đã có rất hiếm các trường hợp phản ứng quá mẫn được báo cáo trên bệnh nhân trước đó đã dung nạp với risperidon hoặc paliperidon đường uống (xem Liều lượng và Cách dùng và Tác dụng ngoại ý).
Nếu phản ứng quá mẫn xảy ra, ngừng dùng INVEGA SUSTENNA; tiến hành các biện pháp hỗ trợ chung thích hợp trên lâm sàng và theo dõi bệnh nhân cho đến khi các triệu chứng và dấu hiệu biến mất (xem Chống chỉ định và Tác dụng ngoại ý).
Tăng đường máu và tiểu đường tuýp II
Tăng đường máu, đái tháo đường, và làm nặng thêm bệnh đái tháo đường có sẵn từ trước đã được báo cáo trong thời gian điều trị với INVEGA SUSTENNA. Đánh giá mối quan hệ giữa việc sử dụng thuốc chống loạn thần không điển hình và các rối loạn đường máu rất phức tạp vì khả năng tăng nguy cơ tiềm ẩn đái tháo đường tuýp II ở bệnh nhân tâm thần phân liệt và tỷ lệ mới mắc của đái tháo đường gia tăng ở quần thể dân số chung. Với những yếu tố nhiễu này cho thấy mối quan hệ giữa sử dụng thuốc chống loạn thần không điển hình và các biến cố bất lợi liên quan tăng đường máu vẫn chưa được biết đầy đủ. Bệnh nhân sử dụng thuốc chống loạn thần không điển hình, bao gồm cả INVEGA SUSTENNA, cần phải được theo dõi các triệu chứng của tăng đường huyết và đái tháo đường tuýp II (xem Tác dụng ngoại ý).
Tăng cân
Tăng cân được quan sát thấy ở bệnh nhân sử dụng thuốc chống loạn thần không điển hình. Khuyến cáo theo dõi cân nặng trên lâm sàng.
Hạ huyết áp thế đứng
Paliperidon có thể gây hạ huyết áp thế đứng ở một số bệnh nhân do hoạt tính chẹn alpha của thuốc. Thận trọng khi dùng INVEGA SUSTENNA cho bệnh nhân đã biết là có bệnh tim mạch (như suy tim, thiếu máu hoặc nhồi máu cơ tim, các rối loạn dẫn truyền), bệnh mạch máu não hoặc những tình trạng làm bệnh nhân hạ huyết áp (như mất nước, giảm thể tích tuần hoàn và sử dụng thuốc điều trị tăng huyết áp).
Co giật
Cũng như những thuốc chống loạn thần khác, cần thận trọng khi dùng INVEGA SUSTENNA cho bệnh nhân mà tiền sử bị co giật và các tình trạng có khả năng làm giảm ngưỡng co giật.
Bệnh nhân cao tuổi bị sa sút trí tuệ
INVEGA SUSTENNA chưa được nghiên cứu ở bệnh nhân cao tuổi bị sa sút trí tuệ.
Tỷ lệ tử vong chung
Trong phân tích gộp cho 17 thử nghiệm lâm sàng có đối chứng, bệnh nhân cao tuổi có sa sút trí tuệ được điều trị bằng thuốc chống loạn thần không điển hình như risperidon, aripiprazol, olanzapin và quetiapin bị tăng tỷ lệ tử vong so với giả dược. Một trong các thuốc này là risperidon, tỷ lệ tử vong là 4% so với 3,1% với giả dược.
Biến cố bất lợi trên mạch máu não
Trong các thử nghiệm đối chứng giả dược trên các bệnh nhân cao tuổi bị sa sút trí tuệ được điều trị bằng thuốc chống loạn thần không điển hình như risperidon, aripiprazol và olanzapin, biến cố bất lợi trên mạch máu não (tai biến mạch máu não và các cơn thiếu máu não thoảng qua), bao gồm cả tử vong có tỷ lệ cao hơn so với giả dược.
Giảm bạch cầu, giảm bạch cầu trung tính và mất hạt bạch cầu hạt
Tác dụng giảm bạch cầu, giảm bạch cầu trung tính và mất bạch cầu hạt đã được báo cáo khi sử dụng thuốc chống loạn thần, kể cả INVEGA SUSTENNA. Mất bạch cầu hạt gặp với tỷ lệ rất hiếm (< 1/10.000 bệnh nhân) trong các theo dõi hậu mãi.
Những bệnh nhân có tiền sử bạch cầu thấp đáng kể trên lâm sàng (WBC) hoặc giảm bạch cầu/giảm bạch cầu hạt trung tính do thuốc cần phải được theo dõi trong những tháng đầu điều trị và phải cân nhắc dừng INVEGA SUSTENNA nếu có dấu hiệu đầu tiên của giảm bạch cầu rõ rệt trên lâm sàng mà không tìm được các yếu tố gây bệnh khác.
Những bệnh nhân bị giảm bạch cầu trung tính rõ rệt trên lâm sàng cần phải theo dõi cẩn thận sốt hoặc các triệu chứng hay dấu hiệu nhiễm trùng và điều trị ngay nếu có các triệu chứng hay dấu hiệu đó xảy ra. Những bệnh nhân bị giảm bạch cầu trung tính nặng (số lượng bạch cầu trung tính tuyệt đối < 1×109/L) thì phải ngừng điều trị INVEGA SUSTENNA và theo dõi cho đến khi số lượng bạch cầu hồi phục.
Huyết khối tĩnh mạch
Các trường hợp huyết khối tĩnh mạch (VTE) cũng đã được báo cáo khi điều trị thuốc chống loạn thần. Vì bệnh nhân sử dụng thuốc chống loạn thần thường có các yếu tố nguy cơ mắc phải của VTE nên tất cả các yếu tố nguy cơ có thể của VTE cần phải được làm rõ trước và trong khi điều trị bằng INVEGA SUSTENNA và các biện pháp phòng ngừa cũng cần được tiến hành.
Bệnh Parkinson và sa sút trí tuệ thể Lewy
Các bác sĩ cần phải cân nhắc nguy cơ và lợi ích khi kê đơn thuốc chống loạn thần, kể cả INVEGA SUSTENNA, cho bệnh nhân Parkinson hoặc sa sút trí tuệ thể Lewy (DLB), vì cả hai bệnh này đều có nguy cơ của Hội chứng thần kinh ác tính do thuốc hướng thần cũng như tăng tính nhạy cảm với các thuốc chống loạn thần. Biểu hiện của tăng tính nhạy cảm này ngoài các triệu chứng ngoại tháp có thể gồm lú lẫn, mất ý thức, bất thường tư thế như thường xuyên bị ngã.
Chứng cương cứng dương vật
Thuốc có tác dụng chẹn alpha-adrenergic có thể gây nên chứng cương cứng dương vật. Chứng cương cứng dương vật đã được báo cáo với paliperidon trong quá trình theo dõi hậu mãi (xem Tác dụng ngoại ý).
Điều hòa thân nhiệt
Rối loạn khả năng làm giảm nhiệt độ của cơ thể cũng là thuộc tính của các thuốc chống loạn thần. Khuyến cáo chăm sóc hợp lý cho các trường hợp điều trị INVEGA SUSTENNA ở trong các môi trường gây tăng nhiệt độ cơ thể như vận động rất nặng, ở môi trường rất nóng, sử dụng đồng thời với thuốc có hoạt tính anticholinergic hoặc đối tượng bị mất nước.
Tác dụng chống nôn
Tác dụng chống nôn gặp trong các nghiên cứu tiền lâm sàng của paliperidon. Tác dụng này, nếu xảy ra ở người, có thể che mờ các dấu hiệu và triệu chứng quá liều của thuốc hoặc các bệnh lý như tắc ruột, hội chứng Reye và u não.
Cách dùng
Cần thận trọng để tránh vô ý tiêm INVEGA SUSTENNA vào mạch máu.
Hội chứng nhão mống mắt trong phẫu thuật
Hội chứng nhão mống mắt trong phẫu thuật (Intraoperative floppy iris syndrome – IFIS) đã được quan sát thấy trong khi phẫu thuật đục thủy tinh thể ở những bệnh nhân được điều trị bằng những thuốc có tác dụng đối kháng alpha1a-adrenergic, kể cả INVEGA SUSTENNA (xem Tác dụng ngoại ý).
IFIS có thể làm tăng nguy cơ biến chứng ở mắt trong và sau khi phẫu thuật. Nên thông báo cho bác sỹ phẫu thuật biết việc đã hoặc đang dùng thuốc có tác dụng đối kháng alpha1a-adrenergic trước cuộc phẫu thuật. Chưa xác định được lợi ích có thể có khi ngừng liệu pháp chẹn alpha1 trước khi phẫu thuật đục thủy tinh thể và phải đánh giá giữa lợi ích và nguy cơ của việc ngừng thuốc chống loạn thần.
Tác động của thuốc trên người lái xe và vận hành máy móc.
INVEGA SUSTENNA có thể ảnh hưởng đến các hoạt động cần phải tỉnh táo và thị giác (xem Tác dụng ngoại ý). Do vậy, bệnh nhân không nên lái xe hay vận hành máy móc cho đến khi tính nhạy cảm cá thể của họ được xác định.
4.5 Sử dụng cho phụ nữ có thai và cho con bú:
Xếp hạng cảnh báo
AU TGA pregnancy category: C
US FDA pregnancy category: NA
Thời kỳ mang thai:
Tính an toàn của paliperidon palmitat dùng tiêm bắp hoặc paliperidon đường uống trên phụ nữ có thai chưa được thiết lập. Không có bất cứ hậu quả gây quái thai nào được ghi nhận trong các nghiên cứu trên động vật thí nghiệm. Những động vật thí nghiệm dùng liều cao paliperidol đường uống cho thấy có tăng nhẹ tỷ lệ thai chết lưu. Nghiên cứu trên chuột cho thấy không thay đổi các chỉ số thai ở chuột có thai khi sử dụng paliperidon palmitat đường tiêm bắp. Liều cao gây độc với chuột mẹ. Chuột con sinh ra không bị ảnh hưởng khi dùng liều uống gấp 20-22 lần liều cao nhất ở người, hoặc với liều tiêm bắp gấp 6 lần liều cao nhất ở người.
Trẻ sơ sinh khi bị phơi nhiễm với thuốc chống loạn thần (bao gồm cả paliperidon) trong 3 tháng cuối của thai kỳ có nguy cơ mắc các triệu chứng ngoại tháp và/hoặc hội chứng cai với các mức độ nặng nhẹ khác nhau sau khi sinh. Những hội chứng này ở trẻ sơ sinh có thể bao gồm các chứng kích thích, tăng trương lực cơ, giảm trương lực cơ, run, ngủ gà, rối loạn hô hấp, hoặc rối loạn dinh dưỡng.
INVEGA SUSTENNA chỉ nên dùng trong thai kỳ nếu lợi ích thu được vượt trội các nguy cơ. Ảnh hưởng của INVEGA SUSTENNA khi chuyển dạ và khi sinh ở người vẫn chưa được biết.
Thời kỳ cho con bú:
Các nghiên cứu trên động vật thí nghiệm với paliperidon và các nghiên cứu trên người với risperidon, cho thấy paliperidon có bài tiết qua sữa mẹ. Do đó, phụ nữ đang dùng INVEGA SUSTENNA không nên cho con bú.
4.6 Tác dụng không mong muốn (ADR):
Các phản ứng bất lợi sẽ được trình bày trong phần này. Các phản ứng bất lợi là các biến cố bất lợi được xem là có liên quan đến việc sử dụng paliperidon dựa trên việc đánh giá toàn diện những thông tin về tác dụng không mong muốn sẵn có. Mối quan hệ nhân quả với paliperidon không thể xác định được chắc chắn trong các trường hợp riêng lẻ. Hơn nữa, những thử nghiệm lâm sàng này được thực hiện trong những điều kiện rất khác nhau, tỷ lệ phản ứng bất lợi được ghi nhận trong những thử nghiệm lâm sàng của một thuốc không thể so sánh trực tiếp với tỷ lệ trong những thử nghiệm lâm sàng của thuốc khác và có lẽ cũng không phản ánh tỷ lệ quan sát được trên thực hành lâm sàng.
Dữ liệu thử nghiệm lâm sàng
Số liệu trong phần này được lấy ra từ dữ liệu thử nghiệm lâm sàng trên tổng số 3817 bệnh nhân người lớn (xấp xỉ 1705 bệnh nhân – năm sử dụng) bị tâm thần phân liệt được sử dụng ít nhất 1 liều INVEGA SUSTENNA trong khoảng liều khuyến cáo từ 25 đến 150 mg và tổng số 510 bệnh nhân tâm thần phân liệt dùng giả dược. Trong tổng số 3817 bệnh nhân được điều trị bằng INVEGA SUSTENNA, 1293 bệnh nhân dùng INVEGA SUSTENNA trong 4 thử nghiệm liều cố định, mù đôi, có đối chứng giả dược (1 nghiên cứu tiến hành trong 9 tuần và 3 nghiên cứu còn lại tiến hành trong 13 tuần), 849 bệnh nhân dùng INVEGA SUSTENNA trong thử nghiệm dự phòng tái phát lâu dài (trung vị phơi nhiễm 229 ngày trong giai đoạn khởi đầu nhãn mở kéo dài 33 tuần của nghiên cứu này, trong số đó có 205 bệnh nhân tiếp tục dùng INVEGA SUSTENNA trong giai đoạn mù đôi, có đối chứng giả dược của nghiên cứu này [trung vị phơi nhiễm 171 ngày]), và 1675 bệnh nhân sử dụng INVEGA SUSTENNA trong 5 thử nghiệm đối chứng không có giả dược, 3 thử nghiệm so sánh không kém hơn, 1 thử nghiệm nhãn mở kéo dài về dược động học và an toàn thuốc và 1 thử nghiệm chuyển vị trí tiêm (cơ delta – cơ mông). Một trong các nghiên cứu kéo dài 13 tuần được khởi đầu với liều INVEGA SUSTENNA 150 mg sau đó duy trì điều trị với liều 25 mg, 100 mg, hoặc 150 mg mỗi 4 tuần.
Phần lớn các phản ứng bất lợi thường ở mức độ từ nhẹ đến trung bình.
Dữ liệu nghiên cứu mù đôi, có đối chứng giả dược
Các phản ứng bất lợi được báo cáo từ ≥ 2% bệnh nhân tâm thần phân liệt điều trị bằng INVEGA SUSTENNA trong 4 thử nghiệm liều cố định, mù đôi, có đối chứng giả dược được mô tả tại Bảng 2.
– xem Bảng 2.

Trong thử nghiệm dự phòng tái phát lâu dài, các loại phản ứng bất lợi, tần suất mắc, và độ nặng trong giai đoạn nghiên cứu nhãn mở của nghiên cứu này được so sánh chung với dữ liệu quan sát được từ 4 nghiên cứu liều cố định, đối chứng với giả dược kéo dài 13 tuần và 9 tuần như đã mô tả trong Bảng 2. Nhìn chung, các loại và độ nặng các phản ứng bất lợi được báo cáo trong giai đoạn mù đôi của nghiên cứu này tương tự với các dữ liệu quan sát được trong giai đoạn nghiên cứu nhãn mở.
Các dữ liệu lâm sàng khác
Paliperidon palmitat được thủy phân thành paliperidon. Paliperidon là một chất chuyển hóa có hoạt tính của risperidon, do vậy đặc tính các phản ứng bất lợi của những hợp chất này (bao gồm cả công thức cho đường uống và đường tiêm) cũng tương tự như nhau. Phần phụ này gồm các phản ứng bất lợi bổ sung được báo cáo trong các thử nghiệm lâm sàng với paliperidon và/hoặc risperidon.
Các phản ứng bất lợi với paliperidon và/hoặc risperidon được báo cáo ≥ 2% số bệnh nhân điều trị với INVEGA SUSTENNA trong cơ sở dữ liệu tổng hợp từ 4 thử nghiệm tâm thần phân liệt mù đôi, có đối chứng giả dược được mô tả chi tiết ở Bảng 3a.
– xem Bảng 3a.

Các phản ứng bất lợi sau dùng paliperidon và/hoặc risperidon được báo cáo từ < 2% số bệnh nhân điều trị với INVEGA SUSTENNA trong cơ sở dữ liệu tổng hơp từ 4 thử nghiệm tâm thần phân liệt, mù đôi có đối chứng giả dược được mô tả chi tiết ở Bảng 3b.
– xem Bảng 3b.

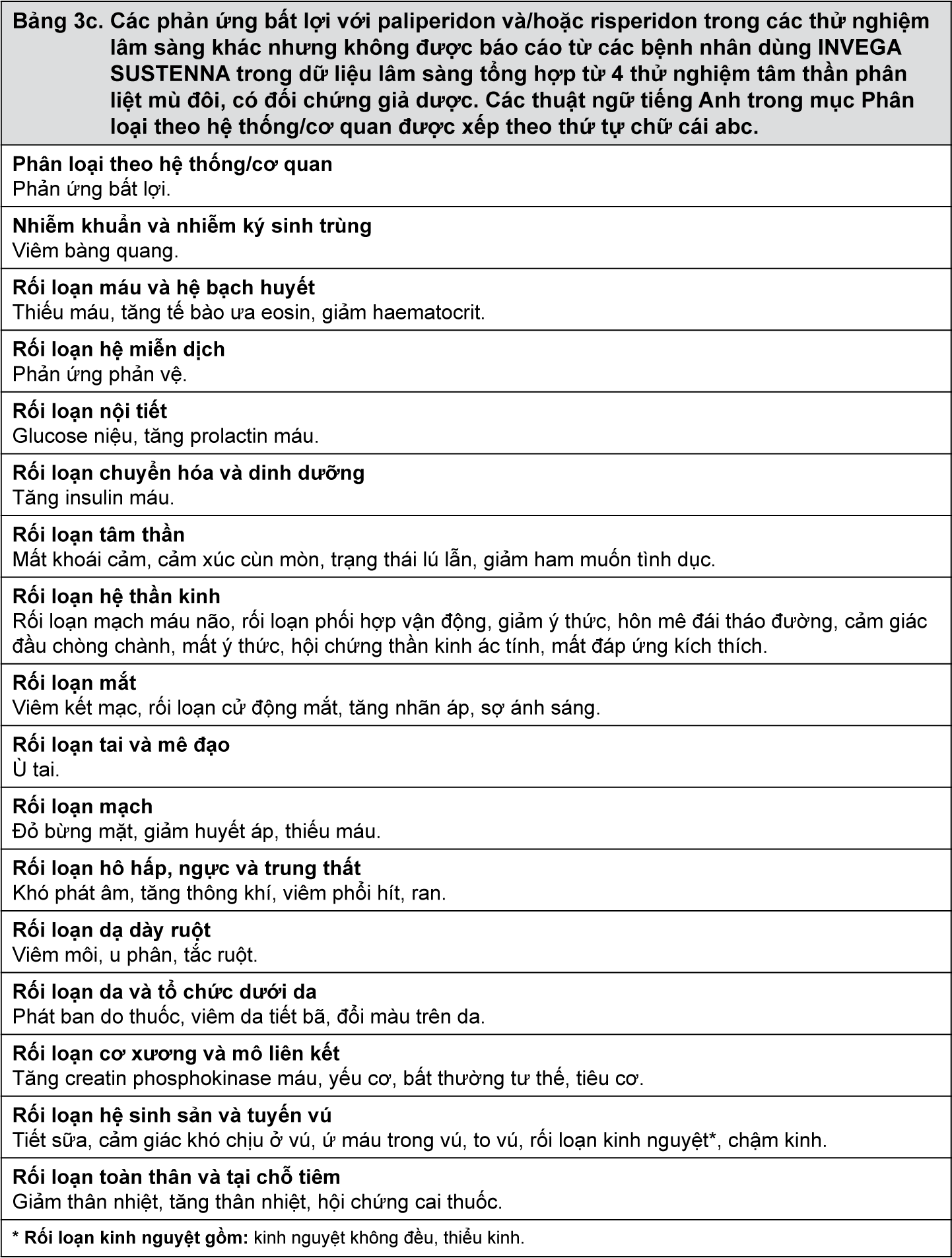
Các phản ứng bất lợi với paliperidon và/hoặc risperidon trong các thử nghiệm lâm sàng khác nhưng không được báo cáo từ các bệnh nhân dùng INVEGA SUSTENNA trong dữ liệu lâm sàng tổng hợp từ 4 thử nghiệm tâm thần phân liệt mù đôi, có đối chứng giả dược được mô tả tại Bảng 3c.
– xem Bảng 3c.
Các biến cố đặc biệt cần lưu ý trong phân loại
Triệu chứng ngoại tháp (EPS)
Dữ liệu tổng hợp từ hai thử nghiệm tâm thần phân liệt, mù đôi, có đối chứng giả dược, liều cố định tiến hành trong 13 tuần (xem Hiệu quả lâm sàng) cho thấy không có sự khác nhau. Hội chứng ngoại tháp do điều trị giữa nhóm chứng và nhóm điều trị bằng INVEGA SUSTENNA. Việc đánh giá EPS bao gồm phân tích gộp các nhóm EPS sau: loạn động, loạn trương lực cơ, tăng động, hội chứng Parkinson và run. Kết quả của nghiên cứu tâm thần phân liệt trong thời gian 13 tuần với liều khởi đầu 150 mg, nghiên cứu tâm thần phân liệt trong thời gian 9 tuần với liều cố định, mù đôi, có đối chứng giả dược và tất cả các giai đoạn của nghiên cứu dự phòng tái phát lâu dài ở bệnh nhân tâm thần phân liệt cho thấy các như dữ liệu ghi nhận được tương tự nhau.
Tăng cân
Tỷ lệ các đối tượng có tăng cân ≥ 7% trọng lượng cơ thể trong nghiên cứu tâm thần phân liệt kéo dài 13 tuần với liều khởi đầu 150 mg cho thấy tăng cân so với ban đầu ≥ 7% gặp phổ biến hơn ở nhóm dùng INVEGA SUSTENNA so với nhóm chứng. Tỷ lệ các đối tượng tăng cân bất thường ≥7% thể hiện xu hướng có liên quan đến liều, với tỷ lệ mắc 5% ở nhóm chứng so với 6%, 8% và 13% ở nhóm dùng INVEGA SUSTENNA các liều 25 mg, 100 mg, và 150 mg tương ứng.
Trong 2 thử nghiệm tâm thần phân liệt tiến hành 13 tuần với liều cố định, mù đôi, có đối chứng giả dược (dữ liệu gộp), tỷ lệ các đối tượng có tăng cân ở mức ≥ 7% trọng lượng cơ thể là 6%, 9%, và 10% ở nhóm sử dụng INVEGA SUSTENNA với các liều 25, 50, và 100 mg tương ứng so với tỷ lệ 2% ở nhóm chứng. Trong thử nghiệm tâm thần phân liệt 9 tuần, liều cố định, mù đôi, có đối chứng giả dược, tỷ lệ gặp là 8% và 6% ở các nhóm dùng INVEGA SUSTENNA với liều 50 và 100 mg tương ứng so với 4% ở nhóm chứng.
Trong giai đoạn chuyển đổi/duy trì mở nhãn kéo dài 33 tuần của thử nghiệm tâm thần phân liệt dự phòng tái phát lâu dài, 12% các đối tượng điều trị bằng INVEGA SUSTENNA đạt tiêu chí đánh giá này (tăng cân ≥ 7% từ giai đoạn mù đôi đến kết thúc nghiên cứu); cân nặng trung bình (SD) thay đổi so với đầu giai đoạn nhãn mở là +0,7 (4,79) kg. Trong giai đoạn mù đôi với những khoảng thời gian thay đổi khác nhau, nhóm sử dụng INVEGA SUSTENNA có tỷ lệ 6% đủ tiêu chuẩn tăng cân (trung bình 171 ngày [dao động từ 1-407 ngày]) so với 3% ở nhóm chứng (trung bình 105 ngày [dao động từ 8-441 ngày]); thay đổi cân nặng trung bình (SD) so với đầu giai đoạn mù đôi là +0,5 (3,83) kg ở nhóm dùng INVEGA SUSTENNA so với -1,0 kg (3,08) ở nhóm chứng. Kết quả tương tự này cũng gặp ở giai đoạn mở rộng nhãn mở của nghiên cứu này.
Thử nghiệm trong phòng thí nghiệm: Prolactin trong huyết thanh
Dữ liệu thu được từ 2 thử nghiệm liều cố định, 13 tuần, mù đôi, có đối chứng giả dược (xem Hiệu quả lâm sàng) cho thấy có tăng giá trị trung vị của prolactin huyết thanh ở cả 2 giới sau điều trị bằng INVEGA SUSTENNA. Kết quả của nghiên cứu trong thời gian 13 tuần với liều khởi đầu 150 mg, và nghiên cứu trong thời gian 9 tuần với liều cố định, mù đôi, có đối chứng giả dược và giai đoạn mù đôi của nghiên cứu dự phòng tái phát đã cung cấp các dữ liệu tương tự nhau.
Kinh nghiệm hậu mãi
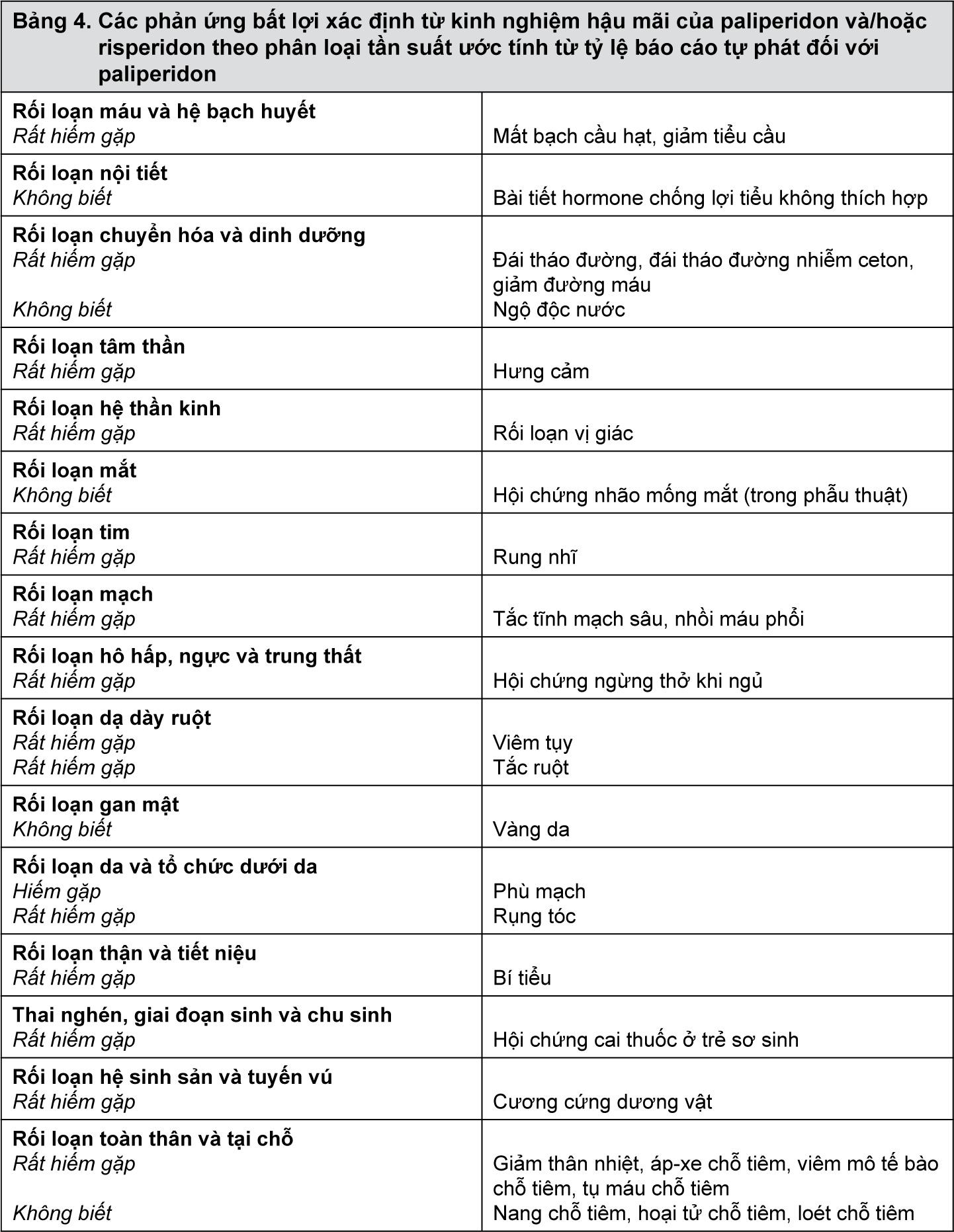
Ngoài các phản ứng bất lợi được báo cáo trong các thử nghiệm lâm sàng như kể trên, các phản ứng bất lợi được ghi nhận với paliperidon và/hoặc risperidon được trình bày trong Bảng 4. Trong bảng này, tần suất gặp được đánh giá theo quy ước sau đây: Rất phổ biến ≥ 1/10, Phổ biến ≥ 1/100 đến < 1/10, Ít gặp ≥ 1/1.000 đến < 1/100, Hiếm gặp ≥ 1/10.000 đến < 1/1.000, Rất hiếm gặp < 1/10.000, bao gồm cả các báo cáo riêng lẻ. Ở Bảng 4, các phản ứng bất lợi được trình bày theo phân loại tần suất gặp dựa vào tỷ lệ các ca báo cáo tự phát.
– xem Bảng 4.
Rất hiếm có trường hợp phản ứng quá mẫn với INVEGA SUSTENNA được báo cáo trong quá trình lưu hành thuốc trên thị trường ở những bệnh nhân trước đó đã dung nạp với risperidon hoặc paliperidon đường uống.
Thông báo cho Bác sĩ những tác dụng không mong muốn gặp phải khi sử dụng thuốc.
4.7 Hướng dẫn cách xử trí ADR:
Ngừng sử dụng thuốc. Với các phản ứng bất lợi nhẹ, thường chỉ cần ngừng thuốc. Trường hợp mẫn cảm nặng hoặc phản ứng dị ứng, cần tiến hành điều trị hỗ trợ (giữ thoáng khí và dùng epinephrin, thở oxygen, dùng kháng histamin, corticoid…).
4.8 Tương tác với các thuốc khác:
Cần thận trọng khi kê đơn đồng thời INVEGA SUSTENNA với các thuốc gây kéo dài khoảng QT.
Do paliperidon palmitat bị thủy phân thành paliperidon (xem Dược động học) nên cần xem xét kết quả của các nghiên cứu với paliperidon đường uống khi đánh giá các khả năng tương tác thuốc-thuốc.
Ảnh hưởng của INVEGA SUSTENNA lên các thuốc khác
Paliperidon không được cho là gây ra những tương tác dược động học quan trọng về mặt lâm sàng với các thuốc bị chuyển hóa bởi các men cytochrom P450. Các nghiên cứu in vitro về các tiểu thể ở gan người cho thấy paliperidon về cơ bản không ức chế sự chuyển hóa của các thuốc bị chuyển hóa bởi các men cytochrom P450, bao gồm: CYP1A2, CYP2A6, CYP2C8/9/10, CYP2D6, CYP2E1, CYP3A4 và CYP3A5. Do đó, paliperidon không được cho là ức chế về mặt lâm sàng sự thải trừ của các thuốc bị chuyển hóa bởi những con đường chuyển hóa này. Paliperidon cũng không được cho là có đặc tính cảm ứng men.
Paliperidon khi dùng ở nồng độ cao là một chất ức chế yếu P-glycoprotein (P-gp). Chưa có dữ liệu in vivo nào và mối liên hệ lâm sàng là chưa rõ.
Do những tác động chủ yếu lên hệ thần kinh trung ương của paliperidon (xem Tác dụng ngoại ý), cần thận trọng khi dùng kết hợp INVEGA SUSTENNA với rượu và các thuốc tác động lên trung ương khác. Paliperidon có thể đối kháng với tác dụng của levodopa và các thuốc đồng vận dopamin khác.
Do khả năng gây hạ huyết áp thế đứng của thuốc (xem Cảnh báo – Hạ huyết áp thế đứng), có thể quan sát thấy tác dụng cộng hợp khi dùng đồng thời INVEGA SUSTENNA với các tác nhân khác có cùng tác dụng này.
Dùng đồng thời paliperidon viên giải phóng kéo dài dạng uống ở trạng thái hằng định (12 mg, 1 lần/ngày) với natri divalproex viên giải phóng kéo dài (500 mg đến 2000 mg, 1 lần/ngày) không ảnh hưởng tới dược động học ở trạng thái hằng định của valproat.
Khó có khả năng xảy ra tương tác dược động học giữa INVEGA SUSTENNA và lithium.
Ảnh hưởng của các thuốc khác tới INVEGA SUSTENNA
Paliperidon không phải là cơ chất của CYP1A2, CYP2A6, CYP2C9, CYP2C19 và CYP3A5. Do đó, khó có khả năng xảy ra tương tác giữa INVEGA SUSTENNA với các chất ức chế hoặc cảm ứng của các men này. Mặc dù các nghiên cứu in vitro chỉ ra rằng CYP2D6 và CYP3A4 có thể có liên quan chút ít tới sự chuyển hóa của paliperidon, không một nghiên cứu in vitro hay in vivo nào cho thấy rằng các men này đóng vai trò đáng kể trong sự chuyển hóa của paliperidon. Các nghiên cứu in vitro cho thấy paliperidon là cơ chất của P-gp.
CYP2D6 chuyển hóa paliperidon đến một mức độ nhất định (xem Dược động học – Chuyển hóa và Thải trừ). Trong một nghiên cứu về tương tác thuốc ở các cá thể khỏe mạnh dùng đồng thời paliperidon và paroxetin là một chất ức chế CYP2D6, không nhận thấy có ảnh hưởng nào về mặt lâm sàng lên dược động học của paliperidon.
Sử dụng đồng thời paliperidon giải phóng kéo dài 1 lần/ngày với carbamazepin 200 mg 2 lần/ngày gây giảm khoảng 37% giá trị trung bình Cmax và AUC ở trạng thái hằng định của paliperidon. Sự giảm đáng kể này là do gia tăng 35% độ thanh thải ở thận của paliperidon, có thể do tác dụng kích thích P-gp thận của carbamazepin. Lượng thuốc chưa chuyển hóa thải trừ qua nước tiểu giảm nhẹ, cho thấy việc sử dụng đồng thời với carbamazepin ít gây ảnh hưởng tới sự chuyển hóa qua CYP cũng như khả dụng sinh học của paliperidon. Khi bắt đầu sử dụng carbamazepin, cần đánh giá lại liều INVEGA SUSTENNA và tăng liều nếu cần thiết. Ngược lại, khi ngừng sử dụng carbamazepin, cần đánh giá lại liều INVEGA SUSTENNA và giảm liều nếu cần thiết.
Paliperidon là một cation ở pH sinh lý, nó được thải trừ ban đầu qua thận dưới dạng chưa chuyển hóa, khoảng một nửa qua hệ thống lọc và một nửa qua bài tiết tích cực. Dùng đồng thời với trimethoprim, một chất ức chế vận chuyển cation qua thận, không ảnh hưởng tới dược động học của paliperidon.
Sử dụng đồng thời liều đơn paliperidon viên nén giải phóng kéo dài dạng uống 12 mg với natri divalproex viên nén giải phóng kéo dài (2 viên 500 mg/ngày) gây tăng khoảng 50% Cmax và AUC của paliperidon. Đây dường như là kết quả của sự tăng hấp thu thuốc qua đường uống. Do không quan sát thấy ảnh hưởng đáng kể nào lên sự thải trừ hệ thống, người ta cho rằng không có tương tác có ý nghĩa về mặt lâm sàng giữa natri divalproex viên nén giải phóng kéo dài và INVEGA SUSTENNA tiêm bắp. Chưa có nghiên cứu nào về tương tác này với INVEGA SUSTENNA.
Khó có khả năng xảy ra tương tác dược động học giữa INVEGA SUSTENNA và lithium.
Dùng đồng thời INVEGA SUSTENNA và risperidon hoặc với paliperidon đường uống
Do paliperidon là chất chuyển hóa có hoạt tính chính của risperidon, cần thận trọng khi dùng INVEGA SUSTENNA cùng với risperidon hoặc paliperidon đường uống trong khoảng thời gian kéo dài. Có ít dữ liệu an toàn liên quan đến sử dụng đồng thời INVEGA SUSTENNA với các thuốc chống loạn thần khác.
4.9 Quá liều và xử trí:
Vì INVEGA SUSTENNA được tiêm bởi cán bộ y tế nên khả năng xảy ra quá liều do bệnh nhân là thấp.
Triệu chứng và dấu hiệu
Nhìn chung, các dấu hiệu và triệu chứng thường là do sự quá mức của các tác động dược lý đã biết của paliperidon, ví dụ: ngủ gà và an dịu, tim đập nhanh và giảm huyết áp, kéo dài khoảng QT và các triệu chứng ngoại tháp. Xoắn đỉnh và rung thất đã được báo cáo khi quá liều đối với paliperidon đường uống. Trong trường hợp quá liều cấp tính, cần phải xem xét đến khả năng dùng nhiều thuốc cùng một lúc.
Điều trị
Cần cân nhắc đến đặc tính giải phóng kéo dài của INVEGA SUSTENNA và thời gian bán thải biểu kiến kéo dài của paliperidon khi đánh giá nhu cầu điều trị và sự hồi phục. Không có thuốc giải độc đặc hiệu cho paliperidon. Nên sử dụng các biện pháp hỗ trợ chung. Tạo và duy trì đường thở thông thoáng và đảm bảo thông khí và cung cấp đủ oxy. Cần theo dõi tim mạch ngay lập tức và nên bao gồm luôn theo dõi điện tâm đồ liên tục để đề phòng trường hợp loạn nhịp tim có thể xảy ra. Giảm huyết áp và trụy mạch cần phải có các biện pháp điều trị phù hợp như truyền tĩnh mạch và/hoặc các thuốc kích thích giao cảm. Trường hợp xuất hiện các triệu chứng ngoại tháp nặng, cần dùng thuốc loại kháng cholinergic. Cần tiếp tục theo dõi và giám sát chặt chẽ cho đến khi bệnh nhân hồi phục hoàn toàn.
5. Cơ chế tác dụng của thuốc :
5.1. Dược lực học:
Nhóm dược lý điều trị: Các thuốc chống loạn thần khác, mã ATC: N05AX13
Cơ chế tác dụng
Paliperidon, hoạt chất chính trong INVEGA SUSTENNA, là một tác nhân hướng thần thuộc nhóm dẫn xuất của benzisoxazol (một thuốc chống loạn thần không điển hình). INVEGA SUSTENNA chứa hỗn hợp racemic của (+)- và (-)- paliperidon.
Paliperidon palmitat bị thủy phân thành paliperidon (xem An toàn tiền lâm sàng). Paliperidon là một chất kháng dopamin D2 trung ương, với tác dụng kháng serotonin 5-HT2A nổi bật. Paliperidon cũng là một chất đối kháng của thụ thể adrenergic alpha 1 và alpha 2 và thụ thể histamin H1. Paliperidon không có ái lực với các thụ thể cholinergic muscarinic hay adrenergic bêta1 và bêta2. Tác dụng dược lý của các đồng phân (+)- và (-)- paliperidon là tương tự nhau cả về số lượng và chất lượng.
Chưa xác định được cơ chế tác dụng của paliperidon, cũng như các thuốc có hiệu quả trong điều trị tâm thần phân liệt khác. Tuy nhiên, người ta cho rằng, thuốc có tác dụng điều trị tâm thần phân liệt thông qua việc kết hợp tác dụng đối kháng các thụ thể dopamin tuýp 2 (D2) và serotonin tuýp 2 (5HT2A). Các tác dụng khác của paliperidon là do sự đối kháng với các thụ thể khác ngoài D2 và 5HT2A.
Ảnh hưởng lên khoảng QT/QC và sinh lý điện tim
Ảnh hưởng lên khoảng QT của paliperidon đường uống được đánh giá thông qua hai nghiên cứu pha 1, mù đôi, ngẫu nhiên, đa trung tâm ở người trưởng thành bị tâm thần thần liệt và rối loạn phân liệt cảm xúc, và trong 3 thử nghiệm đánh giá hiệu quả với liều cố định, tiến hành trong 6 tuần, có đối chứng với hoạt chất và giả dược ở người trưởng thành bị tâm thần phân liệt.
Trong nghiên cứu pha 1 đầu tiên (n=141), bệnh nhân được ngẫu nhiên cho sử dụng hoặc paliperidon đường uống giải phóng tức thì 1 lần/ngày trong 7 ngày (từ 4 đến 8 mg) hoặc liều đơn moxifloxacin (400 mg). Với liều 8 mg paliperidon đường uống giải phóng tức thì 1 lần/ngày (n=50, Cmax ss = 113 ng/mL), giá trị trung bình của nồng độ thuốc tối đa trong huyết tương ở trạng thái hằng định cao gấp 2 lần nồng độ quan sát được khi dùng liều khuyến cáo tối đa 150 mg INVEGA SUSTENNA tiêm cơ delta (ước tính Cmax trung vị là 50 ng/mL). Ở nhóm điều trị với INVEGA SUSTENNA (n=50), trung bình QTcLD (hiệu chỉnh QT so với đường chuẩn trung bình ngày có điều chỉnh) tăng 5,5 mili giây (90% CI: 3,66; 7,25).
Trong nghiên cứu pha 1 thứ hai (n=109), bệnh nhân được ngẫu nhiên cho sử dụng hoặc giả dược, hoặc liều khuyến cáo tối đa của paliperidon đường uống giải phóng kéo dài (12 mg, 1 lần/ngày), sau đó chuyển sang liều cao hơn khoảng khuyến cáo (18 mg, 1 lần/ngày), hoặc một thuốc chứng có hoạt tính cùng nhóm dược lý (400 mg quetiapin, 2 lần/ngày). Ban đầu, trong nghiên cứu không kém hơn kéo dài 10 ngày này, người ta so sánh giữa paliperidon 12 mg giải phóng kéo dài và quetiapin. Khoảng thay đổi trung bình thấp nhất so với ban đầu của QTcLD tại tmax quan sát được của mỗi bệnh nhân dùng 12 mg paliperidon giải phóng kéo dài (Cmax trung bình là 34 ng/mL) thấp hơn khoảng 5,1 ms so với khi dùng liều 400 mg quetiapin 2 lần/ngày (Cmax trung bình 1183 ng/mL) (90% CI: -9,2; -0,9), đạt tiêu chuẩn không kém hơn đã đưa ra là 10 ms. Sự thay đổi trung bình so với ban đầu của QTcLD tại tmax quan sát được ở mỗi bệnh nhân dùng 18 mg paliperidon giải phóng kéo dài (Cmax trung bình là 53 ng/mL) thấp hơn khoảng 2,3 ms so với khi dùng liều 400 mg quetiapin 2 lần/ngày (Cmax trung bình 1183 ng/mL) (90% CI: -6,8; 2,3).
Sự thay đổi trung bình so với ban đầu của QTcLD tại tmax quan sát được của mỗi bệnh nhân dùng 12 mg paliperidon giải phóng kéo dài và bệnh nhân dùng liều 400 mg quetiapin 2 lần/ngày cao hơn so với sự thay đổi trung bình so với ban đầu của QTcLD tại giá trị trung vị tmax quan sát được (của thuốc dùng để so sánh) khi dùng giả dược lần lượt là khoảng 1,5 ms (90% CI: -3,3; 6,2) và 8,0 ms (90% CI: 3,1; 12,9). Sự thay đổi trung bình so với ban đầu của QTcLD tại tmax quan sát được ở mỗi bệnh nhân dùng 18 mg paliperidon giải phóng kéo dài và bệnh nhân dùng liều 400 mg quetiapin 2 lần/ngày cao hơn so với sự thay đổi trung bình so với ban đầu của QTcLD tại tmax trung vị quan sát được (của thuốc dùng để so sánh) khi dùng giả dược lần lượt là khoảng 4,9 ms (90% CI: -0,5; 10,3) và 7,5 ms (90% CI: 2,5; 12,5).
Trong các nghiên cứu này, không bệnh nhân nào có sự thay đổi so với ban đầu vượt quá 60 mili giây hoặc có QTcLD vượt quá 500 mili giây tại bất kì thời điểm nào.
Trong 3 nghiên cứu đánh giá hiệu quả của paliperidon đường uống giải phóng kéo dài với liều cố định trên bệnh nhân tâm thần phân liệt, người ta đo ECG kéo dài ở 15 thời điểm vào các ngày dự kiến (bao gồm thời điểm dự đoán có Cmax) bằng một phương pháp chuẩn. Dựa trên các dữ liệu gộp từ 836 bệnh nhân dùng paliperidon giải phóng kéo dài, 357 bệnh nhân dùng olanzapin và 350 bệnh nhân dùng giả dược, người ta nhận thấy QTcLD trung bình không tăng quá 5 mili giây trong tất cả các nhóm điều trị, ở tất cả các thời điểm. Trong các nghiên cứu này, ở mỗi nhóm điều trị với liều 12 mg paliperidon giải phóng kéo dài và nhóm với olanzapin, có 1 bệnh nhân có sự thay đổi vượt quá 60 mili giây tại một thời điểm (lần lượt là tăng 62 và 110 mili giây).
Trong 4 nghiên cứu đánh giá hiệu quả của INVEGA SUSTENNA với liều cố định trên bệnh nhân tâm thần phân liệt, không bệnh nhân nào có sự thay đổi QTcLD vượt quá 60 mili giây và không bệnh nhân nào có giá trị QTcLD > 500 mili giây tại bất kỳ thời điểm nào. Trong nghiên cứu phòng ngừa tái phát kéo dài trên bệnh nhân tâm thần phân liệt, không bệnh nhân nào có sự thay đổi QTcLD vượt quá 60 mili giây và có 1 bệnh nhân có giá trị QTcLD là 507 mili giây (giá trị khoảng QT được hiệu chỉnh theo Bazett (QTcB) là 483 mili giây); bệnh nhân này có nhịp tim là 45 nhịp/phút.
Hiệu quả lâm sàng
Tâm thần phân liệt
Hiệu quả của INVEGA SUSTENNA trong điều trị tâm thần phân liệt cấp tính được đánh giá qua 4 nghiên cứu ngắn (1 nghiên cứu 9 tuần và 3 nghiên cứu 13 tuần), mù đôi, ngẫu nhiên, có đối chứng giả dược, liều cố định ở bệnh nhân trưởng thành tái phát cấp tính, đáp ứng tiêu chuẩn DSM-IV về tâm thần phân liệt. Bệnh nhân được dùng liều cố định INVEGA SUSTENNA vào các ngày 1, 8 và 36 trong nghiên cứu 9 tuần, thêm ngày 64 ở các nghiên cứu 13 tuần, với khoảng cách 1 tuần cho 2 liều đầu tiên và 4 tuần cho các liều duy trì tiếp theo.
Hiệu quả của thuốc được đánh giá theo Thang điểm Đánh giá hội chứng Âm tính và Dương tính (PANSS) là thang điểm dựa trên 5 yếu tố để đánh giá triệu chứng âm tính và triệu chứng dương tính, tư duy hỗn loạn, thù địch/kích động không kiểm soát và lo lắng/trầm cảm. Chức năng được đánh giá theo thang điểm Thể hiện cá nhân và xã hội (PSP). PSP là thang điểm được đánh giá bởi các nhà lâm sàng để đo các chức năng cá nhân và xã hội trong những hoạt động xã hội hữu ích: làm việc và học tập, các mối quan hệ cá nhân và xã hội, tự chăm sóc bản thân, và những hành vi gây rối, hung hãn. Mức độ rối loạn trong các hoạt động cá nhân, xã hội và tự chăm sóc bản thân được đo bằng mức độ khó khăn để thực hiện các hoạt động đó khi có hay không có sự giúp đỡ của người khác (không có, nhẹ, có biểu hiện, rõ rệt, nặng). Tương tự, mức độ rối loạn trong các hành vi hung hãn được đo bằng sự có hay không có các hành vi này (ví dụ thô lỗ, quát mắng người khác nơi công cộng, đánh vỡ đồ vật, dọa dẫm bằng lời nói, hành hung) và tần suất xuất hiện của những hành vi đó.
Trong 1 nghiên cứu 13 tuần (n=636) so sánh giữa 3 liều cố định INVEGA SUSTENNA (khởi đầu với liều 150 mg tiêm cơ delta, sau đó là 3 liều tiêm cơ delta hoặc cơ mông hoặc 25 mg/4 tuần, hoặc 100 mg/4 tuần, hoặc 150 mg/4 tuần) với giả dược. Sự cải thiện theo tổng điểm PANSS ở cả 3 liều INVEGA SUSTENNA đều cao hơn nhóm dùng giả dược. Trong nghiên cứu này, trừ nhóm dùng liều 25 mg/4 tuần, 2 nhóm còn lại 100 mg/4 tuần, hoặc 150 mg/4 tuần đều có điểm PSP cao hơn có ý nghĩa thống kê so với giả dược. Những kết quả này cho thấy hiệu quả của thuốc trong toàn bộ quá trình điều trị và khả năng cải thiện thang điểm PANSS được quan sát thấy sự khác biệt có ý nghĩa thống kê xuất hiện sớm ngay từ ngày thứ 4 so với nhóm chứng khi dùng INVEGA SUSTENNA với liều 25 mg và từ ngày thứ 8 ở nhóm dùng INVEGA SUSTENNA với liều 150 mg.
Trong 1 nghiên cứu 13 tuần khác (n=349) so sánh giữa 3 liều INVEGA SUSTENNA cố định (50 mg/4 tuần, hoặc 100 mg/4 tuần, hoặc 150 mg/4 tuần) với giả dược, chỉ có nhóm điều trị INVEGA SUSTENNA 100 mg/4 tuần là cho thấy sự ưu việt hơn so với giả dược trong việc cải thiện tổng điểm PANSS. Trong nghiên cứu này, cả nhóm điều trị 50 mg/4 tuần và 100 mg/4 tuần đều tốt hơn giả dược trong cải thiện điểm PSP. Mặc dù nghiên cứu này bao gồm cả liều 150 mg, số lượng cá thể dùng liều này không đủ để có thể đưa ra kết luận liên quan đến hiệu quả của liều.
Trong nghiên cứu thứ 3 tiến hành trong 13 tuần (n=513) so sánh giữa 3 liều cố định INVEGA SUSTENNA (25 mg/4 tuần, hoặc 50 mg/4 tuần, hoặc 100 mg/4 tuần) với giả dược, khả năng cải thiện thang điểm PANSS ở cả 3 nhóm điều trị với INVEGA SUSTENNA đều cao hơn so với giả dược. Trong nghiên cứu này, không nhóm liều paliperidon nào có khả năng cải thiện thang điểm PSP cao hơn có ý nghĩa thống kê so với giả dược.
Trong nghiên cứu 9 tuần (n=197) so sánh giữa 2 liều cố định INVEGA SUSTENNA (50 mg/4 tuần, hoặc 100 mg/4 tuần) với giả dược, sự cải thiện thang điểm PANSS ở cả 2 nhóm liều điều trị với INVEGA SUSTENNA đều cao hơn so với giả dược.
Hiệu quả duy trì kiểm soát triệu chứng và làm chậm tái phát tâm thần phân liệt của INVEGA SUSTENNA được đánh giá trong nghiên cứu dài hạn, mù đôi, có đối chứng giả dược, liều linh hoạt trên 849 người lớn không cao tuổi, đáp ứng tiêu chuẩn DSM-IV về bệnh tâm thần phân liệt. Nghiên cứu này bao gồm giai đoạn nghiên cứu mở, tiến hành trong 33 tuần, điều trị cấp và ổn định, giai đoạn nghiên cứu ngẫu nhiên có đối chứng giả dược nhằm theo dõi sự tái phát và giai đoạn nghiên cứu mở, kéo dài 52 tuần. Trong nghiên cứu này, INVEGA SUSTENNA được dùng hàng tháng với các liều 25, 50, 75, và 100 mg; liều 75 mg chỉ dùng trong giai đoạn nghiên cứu mở, kéo dài 52 tuần. Lúc đầu, các đối tượng được điều trị INVEGA SUSTENNA với liều thay đổi (25-100 mg) trong giai đoạn chuyển tiếp 9 tuần. Để tiếp tục tham gia vào giai đoạn duy trì tiến hành trong 24 tuần, các đối tượng phải có điểm PANSS ≤ 75. Việc điều chỉnh liều chỉ được thực hiện trong 12 tuần đầu của giai đoạn duy trì. Trong giai đoạn mù đôi, linh hoạt về thời gian, bệnh nhân được dùng ngẫu nhiên hoặc INVEGA SUSTENNA mỗi 4 tuần (giá trị trung vị của thời gian điều trị là 171 ngày (dao động từ 1-407 ngày)) với liều giống như họ đang dùng trong giai đoạn ổn định, hoặc dùng giả dược (giá trị trung vị của thời gian điều trị là 105 ngày (dao động từ 8-441 ngày)). Tổng cộng 410 bệnh nhân ổn định được cho dùng ngẫu nhiên hoặc INVEGA SUSTENNA hoặc giả dược cho tới khi xuất hiện các dấu hiệu tái phát tâm thần phân liệt. Sự tái phát được định nghĩa là thời gian cho đến khi có biểu hiện đầu tiên của 1 hoặc một số các dấu hiệu sau: nhập viện để điều trị tâm thần, tổng điểm PANSS tăng ≥ 25% (nếu điểm ban đầu là > 40) hoặc tăng 10 điểm (nếu điểm ban đầu là ≤ 40) trong 2 lần đánh giá liên tiếp; cố ý tự gây thương tích, hành động bạo lực, ý tưởng tự sát/giết người, hoặc có điểm ≥ 5 (nếu điểm tối đa ban đầu ≤ 3) hoặc ≥ 6 (nếu điểm tối đa ban đầu là 4) ở 2 lần đánh giá điểm PANSS liên tiếp, ở các hạng mục P1 (Hoang tưởng), P2 (Tư duy hỗn độn), P3 (Hành vi có tính ảo giác), P6 (Sự đa nghi/ngược đãi), P7 (Thái độ thù địch) hoặc G8 (Sự bất hợp tác). Biến số chính về hiệu quả là thời gian cho đến khi bị tái phát. Một phân tích tạm thời được chuẩn bị trước (sau khi xuất hiện tái phát ở 68 trường hợp) cho thấy bệnh nhân điều trị với INVEGA SUSTENNA có thời gian xuất hiện tái phát dài hơn có ý nghĩa so với nhóm dùng giả dược (Bảng 1), và người ta đã dừng nghiên cứu này sớm do hiệu quả điều trị duy trì đã rõ.
– xem Hình 1.
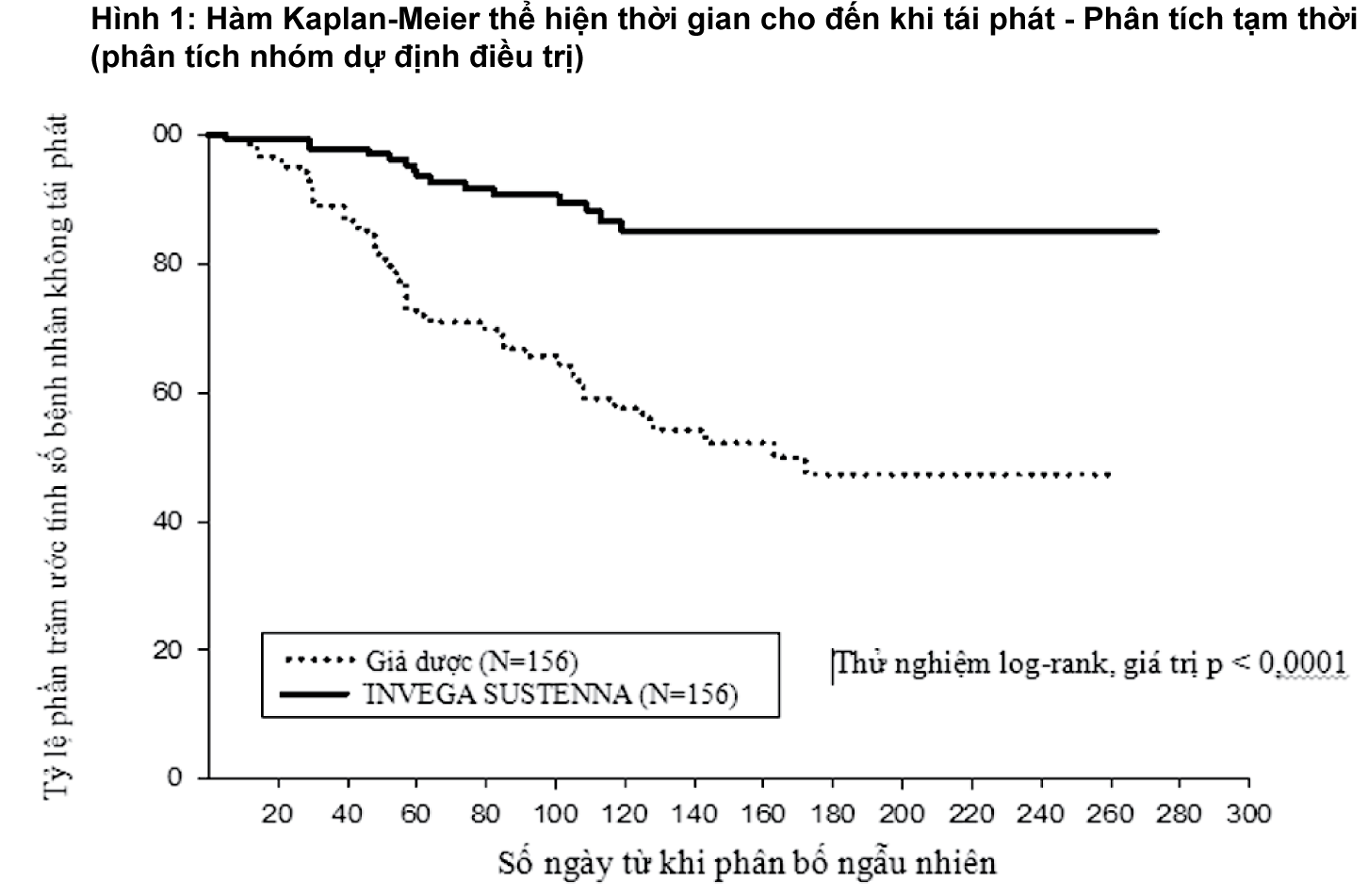
Kết quả phân tích dựa trên dữ liệu cuối kỳ, bao gồm toàn bộ dữ liệu cho đến ngày kết thúc nghiên cứu cũng phù hợp với phân tích hiệu quả ban đầu từ dữ liệu đánh giá tạm thời. Kết quả kiểm tra trên các phân nhóm cho thấy không có sự khác biệt nào có ý nghĩa lâm sàng về khả năng đáp ứng với thuốc giữa giới tính, độ tuổi hay sắc tộc.
Cơ chế tác dụng:
Paliperidone là một chất đối kháng với dopamine D2 tác dụng lên trung ương với hoạt tính đối kháng chủ yếu serotonin 5-HT2A. Paliperidone cũng có tác dụng của một chất đối kháng ở các thụ thể á1 và á2-adrenergic và các thụ thể H1-histaminergic. Paliperidone không có ái lực đối với các thụ thể cholinergic muscarinic hoặc các thụ thể â1 và â2-adrenergic. Hoạt tính dược lý của các chất đối phân (enantiomer) (+)- và (-) – của paliperidone giống nhau về mặt định tính và định lượng.
Cũng như các thuốc khác có hiệu quả đối với tâm thần phân liệt, cơ chế tác dụng của paliperidone chưa được biết. Tuy vậy, người ta cho rằng hoạt tính điều trị của thuốc trong bệnh tâm thần phân liệt được gián tiếp thông qua sự kết hợp của sự đối kháng dopamine typ 2 (D2) và thụ thể serotonin typ 2 (5HT2A).
Sự đối kháng ở các thụ thể khác ngoài D2 và 5HTA2 có thể giải thích một số tác dụng khác của paliperidone.
[XEM TẠI ĐÂY]
5.2. Dược động học:
Hấp thu và phân bố
Do độ tan trong nước rất thấp, nên sau khi tiêm vào cơ, paliperidon palmitat hòa tan từ từ trước khi bị thủy phân thành paliperidon và hấp thu vào hệ thống tuần hoàn. Sau liều đơn tiêm bắp, nồng độ paliperidon trong huyết tương tăng từ từ lên ngưỡng nồng độ tối đa ở tmax trung vị là 13 ngày. Thuốc bắt đầu được giải phóng sớm từ ngày đầu tiên và kéo dài suốt 126 ngày.
Người ta quan sát được trung bình giá trị Cmax cao hơn 28% khi tiêm liều đơn (25-150 mg) vào cơ delta so với tiêm vào cơ mông. Hai liều tiêm khởi đầu vào cơ delta, 150 mg vào ngày 1 và 100 mg vào ngày 8, giúp thuốc đạt được nồng độ điều trị nhanh chóng. Khả năng giải phóng và chế độ dùng liều của INVEGA SUSTENNA giúp duy trì được nồng độ điều trị kéo dài. Tổng nồng độ huyết thanh paliperidon sau khi dùng INVEGA SUSTENNA tỷ lệ thuận với liều dùng trong phạm vi 25-150 mg, và Cmax ít tỷ lệ thuận với liều hơn khi liều dùng vượt quá 50 mg. Tỷ lệ đáy: đỉnh trung bình ở trạng thái ổn định của INVEGA SUSTENNA liều 100 mg khi tiêm cơ mông là 1,8, khi tiêm cơ delta là 2,2. Thời gian bán thải biểu kiến trung vị của paliperidon, sau khi dùng INVEGA SUSTENNA liều từ 25-150 mg nằm trong khoảng từ 25-49 ngày.
Sau khi dùng paliperidon palmitat, các đồng phân (+) và (-) của paliperidon hoán đổi cho nhau, với tỷ lệ giữa AUC của hai dạng là khoảng 1,6-1,8.
Theo một phân tích dân số, thể tích phân bố biểu kiến của paliperidon là 391 L. Tỷ lệ liên kết với protein huyết tương của racemic paliperidon là 74%.
Chuyển hóa và thải trừ
Một tuần sau khi dùng đường uống liều đơn 1 mg 14C-paliperidon giải phóng tức thì, 59% liều này được thải trừ qua nước tiểu dưới dạng chưa chuyển hóa. Điều này cho thấy paliperidon không bị chuyển hóa quá mức ở gan. Khoảng 80% thuốc được thải trừ qua nước tiểu và 11% qua phân. Người ta đã xác định có 4 con đường chuyển hóa thuốc in vivo, trong đó không có con đường nào chuyển hóa quá 6,5% liều: khử alkyl hóa, thủy phân, khử hydro, phân cắt benzisoxazol. Mặc dù các nghiên cứu in vitro chỉ ra rằng CYP2D6 và CYP3A4 có vai trò trong sự chuyển hóa của paliperidon, không có bằng chứng in vivo nào cho thấy rằng các men này đóng vai trò đáng kể trong quá trình chuyển hóa của paliperidon. Các phân tích dược động học quần thể cho thấy không có sự khác biệt rõ ràng nào giữa các chất chuyển hóa mạnh và yếu của cơ chất CYP2D6 trong độ thanh thải biểu kiến của paliperidon sau khi dùng paliperidon đường uống. Các nghiên cứu in vitro về các tiểu thể ở gan người cho thấy paliperidon về cơ bản không ức chế đáng kể sự chuyển hóa của các thuốc bị chuyển hóa bởi các men cytochrom P450, bao gồm: CYP1A2, CYP2A6, CYP2C8/9/10, CYP2D6, CYP2E1, CYP3A4 và CYP3A5.
Các nghiên cứu in vitro cho thấy paliperidon là cơ chất của P-gp và ở nồng độ cao là chất ức chế P-gp yếu. Chưa có dữ liệu in vivo và mối liên hệ lâm sàng là chưa rõ.
So sánh giữa paliperidon palmitat đường tiêm tác dụng kéo dài và paliperidon đường uống giải phóng kéo dài
INVEGA SUSTENNA được thiết kế để giải phóng paliperidon trong khoảng 1 tháng trong khi paliperidon uống dạng giải phóng kéo dài được dùng hàng ngày. Hình 2 cho thấy đặc tính dược động học trung vị trong 5 tuần của paliperidon sau khi dùng INVEGA SUSTENNA với chế độ điều trị khởi đầu theo khuyến cáo so với dùng một viên nén giải phóng kéo dài (6 mg hoặc 12 mg). Chế độ điều trị INVEGA SUSTENNA khởi đầu (150 mg/100 mg tiêm cơ delta vào ngày 1/ngày 8) giúp nhanh chóng đạt được nồng độ paliperidon ổn định khi bắt đầu điều trị mà không cần dùng thêm đường uống.
– xem Hình 2.
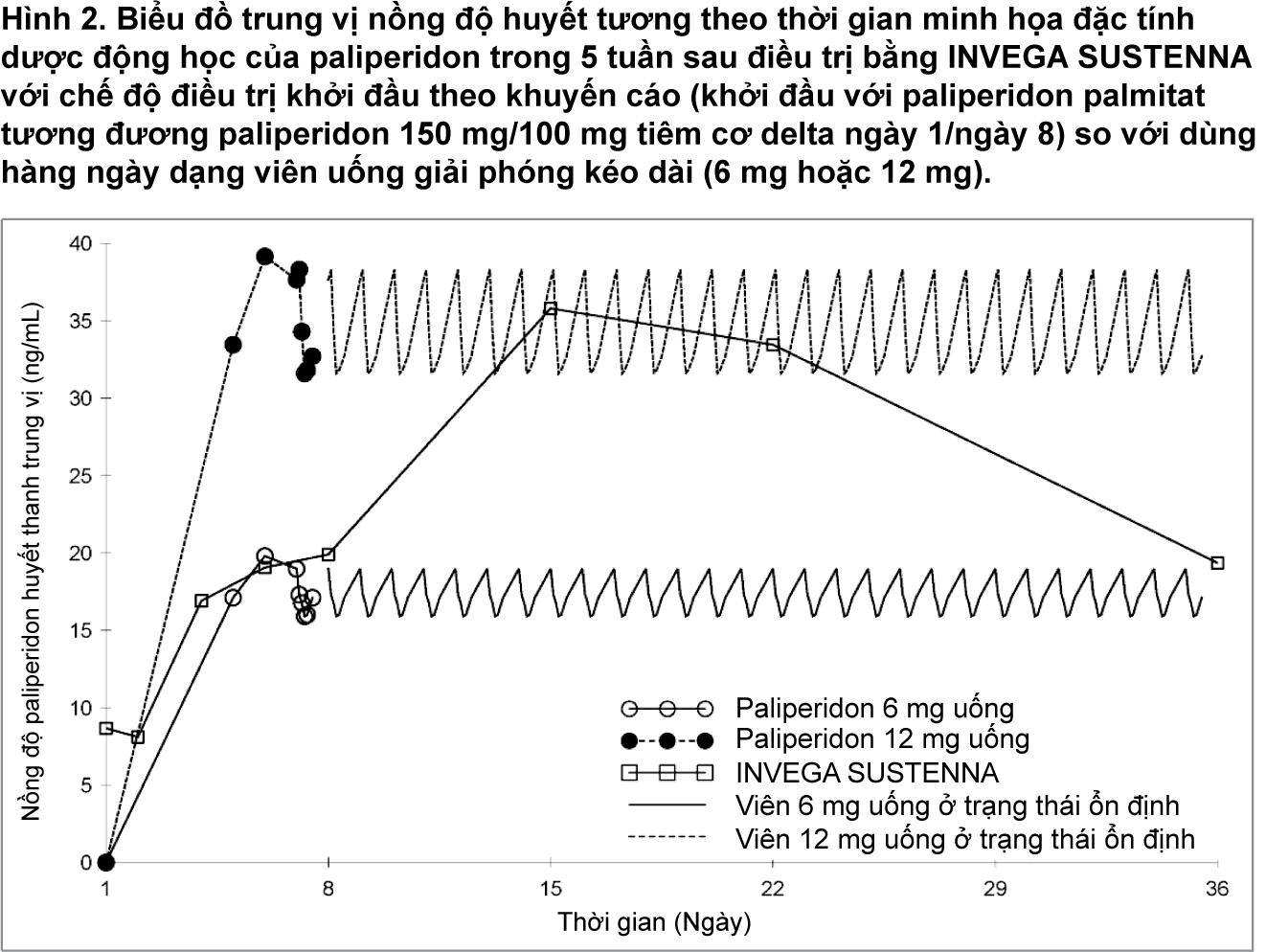
Nói chung, tổng nồng độ INVEGA SUSTENNA ban đầu trong huyết tương nằm trong khoảng quan sát được khi dùng 6-12 mg paliperidon đường uống giải phóng kéo dài. Chế độ liều INVEGA SUSTENNA khởi đầu này giúp bệnh nhân duy trì cửa sổ nồng độ này của khoảng liều 6-12 mg paliperidon đường uống giải phóng kéo dài thậm chí cả trong các ngày trước khi xuống đến nồng độ đáy (ngày 8 và ngày 36). Sự thay đổi cá thể đối với dược động học của paliperidon sau khi giải phóng từ INVEGA SUSTENNA thấp hơn so với paliperidon đường uống giải phóng kéo dài. Do sự khác biệt về trung vị các đặc tính dược động học giữa hai thuốc, cần thận trọng khi so sánh trực tiếp dược động học của 2 thuốc này.
Đối tượng đặc biệt
Người cao tuổi (từ 65 tuổi trở lên)
Không điều chỉnh liều khi chỉ dựa vào tuổi. Tuy nhiên, có thể cần điều chỉnh liều do giảm độ thanh thải creatinin có liên quan tới tuổi (xem Suy thận và Liều dùng và Cách dùng).
Suy thận
Nên giảm liều INVEGA SUSTENNA với bệnh nhân suy thận nhẹ; không khuyến cáo dùng INVEGA SUSTENNA cho bệnh nhân suy thận trung bình hoặc nặng (xem Liều dùng và Cách dùng). Người ta đã nghiên cứu sự thải trừ của liều đơn 3 mg paliperidon đường uống giải phóng kéo dài ở các đối tượng có chức năng thận khác nhau. Sự thải trừ paliperidon giảm khi độ thanh thải creatinin giảm. Độ thanh thải toàn phần của paliperidon giảm trung bình 32% ở bệnh nhân suy thận nhẹ (CrCl = 50 đến < 80 mL/phút), 64% ở bệnh nhân suy thận trung bình (CrCl = 30 đến < 50 mL/phút), và 71% ở bệnh nhân suy thận nặng (CrCl = 10 đến < 30 mL/phút), tương ứng với sự tăng AUCinf trung bình là 1,5, 2,6 và 4,8 lần so với người khỏe mạnh. Dựa trên các quan sát một số lượng giới hạn các bệnh nhân suy thận nhẹ dùng INVEGA SUSTENA và các mô phỏng dược động học, liều INVEGA SUSTENNA khởi đầu khuyến cáo ở những bệnh nhân suy thận nhẹ là 100 mg tiêm cơ delta vào ngày 1 và 75 mg tiêm cơ delta một tuần sau đó; sau đó, tiếp tục tiêm cơ delta hoặc cơ mông hàng tháng (mỗi 4 tuần) 50 mg INVEGA SUSTENNA, thay đổi trong khoảng 25-100 mg tùy thuộc vào khả năng dung nạp của bệnh nhân và/hoặc hiệu quả của thuốc (xem Liều lượng và Cách dùng).
Suy gan
Paliperidon bị chuyển hóa không đáng kể ở gan. Tuy INVEGA SUSTENNA chưa được nghiên cứu ở bệnh nhân suy gan nhưng không cần điều chỉnh liều với bệnh nhân bị suy gan nhẹ hoặc trung bình. Trong một nghiên cứu với các đối tượng bị suy gan mức độ trung bình (Child-Pugh nhóm B), nồng độ paliperidon tự do trong huyết tương tương tự như ở các đối tượng khỏe mạnh. Paliperidon chưa được nghiên cứu ở bệnh nhân suy gan nặng.
Chủng tộc
Dữ liệu phân tích dược động học trên quần thể từ các nghiên cứu với paliperidon đường uống cho thấy không có bằng chứng nào về sự khác biệt về dược động học của paliperidon liên quan tới chủng tộc sau khi dùng INVEGA SUSTENNA.
Giới tính
Không có sự khác biệt nào có ý nghĩa trên lâm sàng giữa nam và nữ giới.
Hút thuốc
Kết quả nghiên cứu in vitro sử dụng men gan người cho thấy paliperidon không phải là cơ chất của CYP1A2; do đó, hút thuốc không ảnh hưởng tới dược động học của paliperidon. Cùng với kết quả nghiên cứu in vitro này, kết quả đánh giá trên quần thể cũng cho thấy không có sự khác biệt nào về dược động học giữa người có hút thuốc và không hút thuốc.
5.3 Giải thích:
Chưa có thông tin. Đang cập nhật.
5.4 Thay thế thuốc :
Chưa có thông tin. Đang cập nhật.
*Lưu ý:
Các thông tin về thuốc trên Pharmog.com chỉ mang tính chất tham khảo – Khi dùng thuốc cần tuyệt đối tuân theo theo hướng dẫn của Bác sĩ
Chúng tôi không chịu trách nhiệm về bất cứ hậu quả nào xảy ra do tự ý dùng thuốc dựa theo các thông tin trên Pharmog.com
6. Phần thông tin kèm theo của thuốc:
6.1. Danh mục tá dược:
–
6.2. Tương kỵ :
INVEGA SUSTENNA không nên trộn với bất kỳ thuốc nào khác hay pha loãng và chỉ được tiêm bắp trực tiếp từ bơm tiêm đã đóng sẵn thuốc.
6.3. Bảo quản:
Nơi khô, tránh ánh sáng, nhiệt độ dưới 30°C.
6.4. Thông tin khác :
An toàn tiền lâm sàng
Độc tính
Cũng như các thuốc có đối kháng thụ thể dopamin D2 khác, paliperidon palmitat tiêm bắp cũng như paliperidon đường uống làm tăng prolactin huyết thanh trong các nghiên cứu về độc tính liều nhắc lại.
Trong nghiên cứu độc tính tiến hành trong 7 tuần trên chuột non với paliperidon các liều uống 0,16, 0,63 và 2,5 mg/kg/ngày, những liều này gấp 0,12; 0,5 và 1,8 lần liều uống cao nhất được khuyến cáo dùng cho người là 12 mg/ngày đối với thanh thiếu niên tính theo mg/m2, không quan sát thấy ảnh hưởng đến sự phát triển, sự trưởng thành giới tính và khả năng sinh sản. Liều uống lên tới 2,5 mg/kg/ngày không gây tổn thương đến sự phát triển hành vi thần kinh ở cả chuột cái và chuột đực, ngoại trừ sự ảnh hưởng lên học tập và trí nhớ ở chuột cái khi dùng liều 2,5 mg/kg/ngày. Ảnh hưởng này không còn quan sát thấy khi dừng điều trị.
Trong nghiên cứu tiến hành trong 40 tuần trên chó non với risperidon với các liều uống (được quy đổi sang paliperidon) 0,31; 1,25 và 5 mg/kg/ngày, không có ảnh hưởng xấu lên sự trưởng thành giới tính ở liều 0,31 và 1,25 mg/kg/ngày. Sự phát triển chiều dài của xương không bị ảnh hưởng ở liều 0,31 mg/kg/ngày; các ảnh hưởng quan sát được khi dùng liều 1,25 và 5 mg/kg/ngày.
Gây ung thư
Khả năng gây ung thư khi dùng paliperidon palmitat theo đường tiêm bắp được đánh giá trên chuột cống. Ung thư biểu mô tuyến vú tăng có ý nghĩa thống kê trên chuột cái ở các liều 10, 30 và 60 mg/kg/tháng. Ở chuột đực, u tuyến vú và ung thư biểu mô tuyến vú tăng có ý nghĩa thống kê ở liều 30 và 60 mg/kg/tháng – cao gấp 1,2 và 2,2 mức độ phơi nhiễm ở liều khuyến cáo cao nhất dùng cho người là 150 mg INVEGA SUSTENNA.
Khả năng gây ung thư của paliperidon đường uống, một chất chuyển hóa có hoạt tính của risperidon, được đánh giá dựa trên các nghiên cứu với risperidon trên chuột nhắt và chuột cống. Risperidon được sử dụng với liều lên tới 10 mg/kg/ngày trong 18 tháng trên chuột nhắt và trong 25 tháng trên chuột cống.
U tuyến yên, u tụy nội tiết và ung thư biểu mô tuyến vú tăng có ý nghĩa thống kê. U vú, u tuyến yên và u tụy nội tiết đã được ghi nhận ở loài gặm nhấm sau khi dùng lâu dài các thuốc chống loạn thần khác và được coi là qua trung gian của tác động đối kháng thụ thể dopamin D2 kéo dài. Liên quan giữa các phát hiện u này trên động vật gặm nhấm với nguy cơ trên người vẫn chưa được biết.
Đột biến gen
Không có bằng chứng cho thấy paliperidon có khả năng gây đột biến gen trong thử nghiệm đột biến ngược Ames, thử nghiệm u lympho trên chuột nhắt, hoặc thử nghiệm tiểu thể nhân trên chuột cống. Paliperidon palmitat được cho thấy không có đặc tính gây độc gen qua thử nghiệm đột biến ngược Ames và thử nghiệm u lympho trên chuột nhắt.
Giảm khả năng sinh sản
Mặc dù paliperidon dạng uống có ảnh hưởng đến prolactin và điều hòa thần kinh trung ương nhưng khả năng sinh sản trên chuột cái và chuột đực vẫn không bị ảnh hưởng. Với liều gây độc cho thai kỳ cho thấy có giảm nhẹ số lượng phôi sống ở chuột cống cái.
6.5 Tài liệu tham khảo:
MIMS Việt Nam
HDSD Thuốc Invega Sustenna.
7. Người đăng tải /Tác giả:
Bài viết được sưu tầm hoặc viết bởi: Bác sĩ nhi khoa – Đỗ Mỹ Linh.
Kiểm duyệt , hiệu đính và đăng tải: PHARMOG TEAM


