Vaccine ngừa Covid Astrazeneca là gì ? Dưới đây là nội dung tờ hướng dẫn sử dụng gốc của Vaccine ngừa Covid Astrazeneca (Thông tin bao gồm liều dùng, cách dùng, chỉ định, chống chỉ định, thận trọng, dược lý…)
1. Tên hoạt chất và biệt dược:
Hoạt chất : COVID-19 Vaccine (Vaccine ngừa Covid)
Phân loại: Vaccines, Huyết thanh và Globulin miễn dịch.
Nhóm pháp lý: Vắc-xin/Sinh phẩm y tế
Mã ATC (Anatomical Therapeutic Chemical): J07BX03.
Biệt dược gốc:
Biệt dược: COVID-19 Vaccine AstraZeneca suspension for injection, COVID-19 Vaccine, Vắc xin AstraZeneca, Vaccine AstraZeneca
Hãng sản xuất : Catalent Anagni S.R.L-Y; CP Pharmaceuticals Limited – Anh.l; IDT Biologika GmbH – Đức (phát triển và phân phối bởi AstraZeneca)
2. Dạng bào chế Hàm lượng:
Dạng thuốc và hàm lượng
Sản phẩm thuốc này phải được theo dõi thêm. Điều này sẽ cho phép xác định nhanh chóng các thông tin an toàn mới. Các chuyên gia chăm sóc sức khỏe được yêu cầu báo cáo bất kỳ phản ứng phụ nghi ngờ nào. Xem phần 4.8 để biết cách báo cáo phản ứng phụ.
Dạng bào chế: Dung dịch tiêm/Hỗn dịch tiêm.
Một liều (0,5 ml) chứa: vắc xin COVID-19 (ChAdOxl-S tái tổ hợp) không ít hơn 2,5 x 10^8 đơn vị lây nhiễm (Inf.U).
* Được sản xuất trong tế bào thận phôi người (HEK) 293 đã được biến đổi gen và bằng công nghệ DNA tái tổ hợp.
Sản phẩm này có chứa các sinh vật biến đổi gen (GMO).
Mỗi liều (0,5 ml) chứa khoảng 2 mg ethanol.
Hỗn dịch không màu đến hơi nâu, trong đến hơi đục với độ pH là 6,6.
Thuốc tham khảo:
| COVID-19 VACCINE ASTRAZENECA | ||
| Mỗi 0,5 ml liều tiêm có chứa: | ||
| ChAdOxl-S tái tổ hợp | …………………………. | ≥ 2,5 x 10^8 Inf.U * |
| Tá dược | …………………………. | vừa đủ (Xem mục 6.1) |
3. Video by Pharmog:
[VIDEO DƯỢC LÝ]
————————————————
► Kịch Bản: PharmogTeam
► Youtube: https://www.youtube.com/c/pharmog
► Facebook: https://www.facebook.com/pharmog/
► Group : Hội những người mê dược lý
► Instagram : https://www.instagram.com/pharmogvn/
► Website: pharmog.com
4. Ứng dụng lâm sàng:
4.1. Chỉ định:
Vắc xin phòng ngừa COVID-19 AstraZeneca được chỉ định tiêm chủng chủ động để phòng ngừa COVID-19 do SARS-CoV-2 gây ra, ở những người từ 18 tuổi trở lên
Việc sử dụng vắc xin này phải tuân theo các khuyến cáo chính thức.
4.2. Liều dùng Cách dùng:
Cách dùng :
Vắc xin phòng ngừa COVID-19 AstraZeneca chỉ dùng để tiêm bắp, tốt nhất là tiêm vào cơ delta của cánh tay trên.
Không tiêm vắc xin trong mạch, tiêm dưới da hoặc tiêm trong da.
Không được trộn vắc xin trong cùng một ống tiêm với bất kỳ vắc xin hoặc sản phẩm thuốc nào khác.
Để biết các biện pháp phòng ngừa trước khi sử dụng vắc xin, hãy xem phần thận trọng
Để biết hướng dẫn về cách xử lý và thải bỏ, hãy xem phần hướng dẫn về cách xử lý và thải bỏ.
Hướng dẫn về cách xử lý và thải bỏ
Vắc xin này cần được chuyên gia y tế xử lý bằng kỹ thuật vô trùng để đảm bảo tính vô trùng của mỗi liều.
Không sử dụng vắc xin này sau ngày hết hạn được ghi trên nhãn sau EXP. Ngày hết hạn là ngày cuối cùng của tháng hết hạn.
Lọ đa liều chưa mở nên được bảo quản trong tủ lạnh (2 ° C – 8 ° C). Không để đóng băng.
Giữ các lọ trong thùng carton để tránh ánh sáng.
Vắc xin phải được kiểm tra bằng mắt thường để tìm các biến đổi như dị vật/các hạt và sự đổi màu trước khi sử dụng. Vắc xin phòng ngừa COVID-19 AstraZeneca là hỗn dịch không màu đến hơi nâu, trong đến hơi đục. Bỏ lọ nếu thấy bị đổi màu hoặc quan sát thấy các hạt. Không được lắc. Không pha loãng hỗn dịch.
Không được trộn vắc xin trong cùng một ống tiêm với bất kỳ vắc xin hoặc sản phẩm thuốc nào khác.
Liệu trình tiêm chủng vắc xin phòng ngừa COVID-19 AstraZeneca bao gồm hai liều riêng biệt, mỗi liều 0,5 ml. Liều thứ hai nên được thực hiện trong khoảng thời gian từ 4 đến 12 tuần sau liều đầu tiên. Những người đã được tiêm liều đầu tiên của Vắc xin phòng ngừa COVID-19 AstraZeneca nên tiêm liều thứ hai cùng loại để hoàn thành liệu trình tiêm chủng.
Mỗi liều vắc xin 0,5 ml được rút vào ống tiêm để tiêm để tiêm bắp, tốt nhất là tiêm vào cơ delta của bắp tay. Sử dụng kim tiêm mới khi tiêm.
Chất lỏng vẫn còn thừa trong lọ sau khi rút liều cuối cùng là điều bình thường. Mỗi lọ được bổ sung thêm một phần để đảm bảo có thể chia đủ 8 liều (lọ 4 ml) hoặc 10 liều (lọ 5 ml) 0,5 ml. Không gộp vắc xin thừa từ nhiều lọ. Bỏ bất các phần vắc xin nào không sử dụng.
Tính ổn định khi sử dụng về mặt hóa học và vật lý đã được chứng minh từ thời điểm mở lọ (lần đâm kim đầu tiên) đến khi sử dụng là không quá 48 giờ trong tủ lạnh (2 ° C – 8 ° C). Trong khoảng thời gian này, sản phẩm có thể được giữ và sử dụng ở nhiệt độ lên đến 30 ° C trong thời gian tối đa 6 giờ. Sau khoảng thời gian này, sản phẩm phải được loại bỏ. Không bỏ lại vào tủ lạnh.
Thải bỏ
Vắc xin phòng ngừa COVID -19 AstraZeneca chứa các sản phẩm biến đổi gen (GMO). Bất kỳ nguyên liệu vắc xin hoặc phần thừa vắc xin nào không sử dụng phải được xử lý theo hướng dẫn của địa phương đối với sản phẩm biến đổi gen hoặc chất thải nguy hại sinh học. Các chỗ tràn/đổ vỡ phải được khử trùng bằng cách sử dụng các chất có hoạt tính chống lại adenovirus.
Liều dùng:
Người từ 18 tuổi trở lên
Liệu trình tiêm chủng vắc xin phòng ngừa COVID-19 AstraZeneca bao gồm hai liều riêng biệt, mỗi liều 0,5 ml. Liều thứ hai nên được thực hiện trong khoảng thời gian từ 4 đến 12 tuần (28 đến 84 ngày) sau liều đầu tiên (xem phần dược lý).
Không có dữ liệu về khả năng thay thế lẫn nhau của Vắc xin phòng ngừa COVID-19 AstraZeneca với các vắc xin phòng ngừa COVID-19 khác để hoàn thành liệu trình tiêm chủng. Những người đã tiêm liều đầu tiên bằng vắc xin phòng ngừa COVID-19 AstraZeneca nên tiêm liều thứ hai cũng là vắc xin phòng ngừa COVID-19 AstraZeneca để hoàn thành liệu trình tiêm chủng.
Trẻ em
Tính an toàn và hiệu quả của Vắc xin ngừa COVID -19 AstraZeneca ở trẻ em và thanh thiếu niên (dưới 18 tuổi) vẫn chưa được thiết lập.
Người cao tuổi
Không cần điều chỉnh liều. Xem thêm phần thận trọng và dược lý.
4.3. Chống chỉ định:
Quá mẫn với hoạt chất hoặc với bất kỳ tá dược nào của Vắc xin
4.4 Thận trọng:
Truy xuất nguồn gốc sản phẩm
Để nâng cao khả năng truy xuất nguồn gốc của Vắc xin, cần ghi rõ tên và số lô của lọ vắc xin được sử dụng
Phản ứng quá mẫn và Shock phản vệ
Luôn sẵn sàng để xử lý và theo dõi y tế trong trường hợp xảy ra phản vệ sau khi sử dụng vắc xin. Nên theo dõi sát ít nhất 15 phút sau khi tiêm chủng. Không nên tiêm liều thứ hai cho những người đã bị sốc phản vệ với liều đầu tiên của Vắc xin ngừa COVID -19 AstraZeneca.
Biểu hiện liên quan đến lo lắng
Các biểu hiện liên quan đến lo lắng, bao gồm ngất do phản xạ thần kinh phế vị, tăng thông khí hoặc các biểu hiện liên quan đến căng thẳng có thể xảy ra khi tiêm vắc-xin bắt nguồn từ tâm lý sợ tiêm (kim tiêm). Điều quan trọng là phải có các biện pháp dự phòng để tránh bị thương do ngất xỉu.
Bệnh nhân mắc bệnh khác đồng thời
Việc tiêm chủng nên được xem xét hoãn lại ở những người đang bị sốt cao do các bệnh cấp tính hoặc nhiễm trùng cấp. Tuy nhiên, có thể không cần hoãn việc tiêm chủng khi đang mắc nhiễm trùng nhẹ và/hoặc sốt nhẹ.
Giảm tiểu cầu và rối loạn đông máu
Cũng như các dạng tiêm bắp khác, nên thận trọng khi tiêm vắc-xin cho những người đang điều trị bằng thuốc chống đông máu hoặc những người bị giảm tiểu cầu hoặc bất kỳ rối loạn đông máu nào (ví dụ như bệnh máu khó đông) vì có thể xảy ra chảy máu hoặc bầm tím sau khi tiêm bắp ở những người này.
Người bị suy giảm miễn dịch
Chưa đánh giá được hiệu quả, tính an toàn và tính sinh miễn dịch của vắc xin ở những người bị suy giảm miễn dịch, kể cả những người đang điều trị bằng thuốc ức chế miễn dịch. Hiệu quả của Vắc xin ngừa COVID-19 AstraZeneca có thể kém hơn ở những người bị suy giảm miễn dịch.
Thời gian bảo vệ
Thời gian bảo vệ của vắc-xin vẫn chưa được biết vì nó vẫn đang được xác định bằng các thử nghiệm lâm sàng trên người.
Sự hạn chế về hiệu quả của vắc xin
Hiệu quả của Vắc xin bắt đầu xuất hiện khoảng 3 tuần sau khi tiêm liều đầu tiên Vắc xin phòng COVID-19 AstraZeneca. Do đó những người tiêm mũi vắc xin đầu tiên có thể không được bảo vệ đầy đủ cho đến 15 ngày sau khi tiêm liều thứ hai. Như tất cả các loại vắc xin khác, việc tiêm vắc xin phòng COVID-19 AstraZeneca có thể không bảo vệ được tất cả những người được tiêm.
Dữ liệu thử nghiệm lâm sàng hiện có không cho phép ước tính hiệu quả của vắc xin ở những đối tượng trên 55 tuổi.
Cảnh báo về tá dược
Natri: Sản phẩm thuốc này chứa ít hơn 1 mmol natri (23 mg) trên mỗi liều 0,5 ml, nghĩa là về cơ bản “không chứa natri”.
Ethanol: Sản phẩm thuốc này chứa 2 mg cồn (etanol) mỗi liều 0,5 ml. Một lượng nhỏ rượu trong sản phẩm thuốc này sẽ không có bất kỳ ảnh hưởng đáng chú ý nào.
Tác động của thuốc trên người lái xe và vận hành máy móc.
Vắc xin phòng ngừa COVID-19 AstraZeneca không có hoặc ảnh hưởng không đáng kể đến khả năng lái xe và sử dụng máy móc. Tuy nhiên, một số phản ứng bất lợi được đề cập trong mục tác dụng không mong muốn có thể tạm thời ảnh hưởng đến khả năng lái xe hoặc sử dụng máy móc.
4.5 Sử dụng cho phụ nữ có thai và cho con bú:
Xếp hạng cảnh báo
AU TGA pregnancy category: NA
US FDA pregnancy category: NA
Thời kỳ mang thai:
Kinh nghiệm sử dụng vắc xin phòng ngừa COVID-19 AstraZeneca ở phụ nữ có thai còn hạn chế.
Các nghiên cứu về độc tính sinh sản của động vật vẫn chưa được hoàn thành. Dựa trên kết quả từ nghiên cứu sơ bộ, không có ảnh hưởng nào đến sự phát triển của thai nhi.
Chỉ nên cân nhắc sử dụng Vắc xin ngừa COVID-19 AstraZeneca trong thời kỳ mang thai khi lợi ích vượt trội hơn bất kỳ nguy cơ tiềm ẩn nào cho mẹ và thai nhi.
Khả năng sinh sản
Các nghiên cứu trên động vật không chỉ ra tác hại trực tiếp hoặc gián tiếp đối với độc tính sinh sản.
Thời kỳ cho con bú:
Người ta chưa biết liệu Vắc xin phòng ngừa COVID-19 AstraZeneca có được bài tiết qua sữa mẹ hay không
4.6 Tác dụng không mong muốn (ADR):
Tóm tắt tính an toàn
Tính an toàn tổng thể của Vắc xin phòng ngừa COVID-19 AstraZeneca dựa trên phân tích tạm thời của dữ liệu tổng hợp từ bốn thử nghiệm lâm sàng được thực hiện ở Vương quốc Anh, Brazil và Nam Phi. Tại thời điểm phân tích, 23.745 người tham gia ≥18 tuổi đã được chọn ngẫu nhiên và tiêm vắc xin phòng ngừa COVID-19 AstraZeneca hoặc giả dược. Trong số này, 12.021 người đã nhận được ít nhất một liều vắc-xin COVID-19 AstraZeneca và 8.266 đã nhận được hai liều. Thời gian theo dõi trung bình là 62 ngày sau liều 2.
Các phản ứng có hại được báo cáo thường xuyên nhất là nhạy cảm chỗ tiêm (63,7%), đau chỗ tiêm (54,2%), nhức đầu (52,6%), mệt mỏi (53,1%), đau cơ (44,0%), khó chịu (44,2%), sốt nóng (bao gồm hơi sốt (33,6%) và sốt> 38 ° C (7,9%)), ớn lạnh (31,9%), đau khớp (26,4%) và buồn nôn (21,9%). Phần lớn các phản ứng có hại ở mức độ nhẹ đến trung bình và thường hết trong vài ngày sau khi tiêm chủng. Khi so sánh với liều đầu tiên, các phản ứng ngoại ý được báo cáo sau liều thứ hai nhẹ hơn và ít xảy ra hơn.
Khả năng phản ứng thường nhẹ hơn và ít gặp hơn ở người lớn tuổi (≥65 tuổi).
Hồ sơ an toàn là nhất quán giữa những người tham gia có hoặc không có bằng chứng trước đó về nhiễm SARS-CoV-2 lúc đầu; số người tham gia có xét nghiệm SARS-CoV-2 dương tính tại thời điểm ban đầu là 718 người (3,0%).
Bảng tổng hợp các tác dụng phụ
Sắp xếp các biến có bất lợi, ở tất cả các mức độ, được liệt kê theo phân loại hệ cơ quan MedDRA, tần suất và mức độ nghiêm trọng. Các quy ước đưới đây được sử dụng để phân loại tần suất: rất phổ biến > 1/10; phổ biến > 1/100 đến < 1/10; không phổ biến > 1/1.000 đến < 1/100; hiếm gặp > 1/10.000 đến < 1/1.000; rất hiếm gặp < 1/10.000 và chưa biết rõ (không thể ước tính được từ các dữ liệu hiện có).
Bảng 1: Phản ứng có hại của thuốc
| MedDRA SOC | Tần suất | Phản ứng có hại |
| Rối loạn hệ thống bạch huyết và máu | Không phổ biến | Bệnh nổi hạch |
| Rối loạn chuyển hóa và dinh dưỡng | Không phổ biến | Giảm cảm giác thèm ăn |
| Rối loạn hệ thần kinh | Rất phổ biến | Nhức đầu |
| Không phổ biến | Chóng mặt
Buồn ngủ |
|
| Rối loạn tiêu hóa | Rất phổ biến | Buồn nôn |
| Phổ biến | Nôn mửa
Tiêu chảy |
|
| Rối loạn da và mô dưới da | Không phổ biến | Tăng tiết mồ hôi
Ngứa Phát ban |
| Rối loạn cơ xương và mô liên kết | Rất phổ biến | Đau cơ
Đau khớp |
| Các rối loạn chung và rối loạn tại chỗ tiêm | Rất phổ biến | Nhạy cảm chỗ tiêm
Đau chỗ tiêm Nóng đỏ chỗ tiêm Ngứa chỗ tiêm Vết bầm tím tại chỗ tiêm (a) Mệt mỏi Khó chịu Hơi sốt Ớn lạnh |
| Phổ biến | Chỗ tiêm sưng tấy
Ban đỏ tại chỗ tiêm Sốt (b) |
(a) Vết bầm tím tại chỗ tiêm bao gồm cả tụ máu tại chỗ tiêm (không phổ biến)
(b) Sốt đo được ≥38 ° C
Thông báo cho Bác sĩ những tác dụng không mong muốn gặp phải khi sử dụng thuốc.
4.7 Hướng dẫn cách xử trí ADR:
Luôn chuấn bị sẵn một số thuốc như adrenalin (1:1 000) và những trang bị cần thiết cho điều trị sốc phản vệ nếu xảy ra (oxygen, máy trợ hô hấp).
4.8 Tương tác với các thuốc khác:
Không có nghiên cứu tương tác nào được thực hiện.
Việc dùng đồng thời vắc xin phòng ngừa COVID-19 AstraZeneca với các vắc xin khác chưa được nghiên cứu.
4.9 Quá liều và xử trí:
Không có phương pháp điều trị cụ thể cho trường hợp quá liều với Vắc xin phòng ngừa COVID-19 AstraZeneca. Trong trường hợp quá liều, người bệnh phải được theo dõi và điều trị triệu chứng khi cần thiết.
5. Cơ chế tác dụng của thuốc :
5.1. Dược lực học:
Nhóm dược lý: Vắc xin, huyết thanh và globulin miễn dịch, mã ATC: J07BX03
Cơ chế tác dụng (Cho cán bộ y tế)
Vắc xin phòng ngừa COVID-19 AstraZeneca là một loại vắc xin đơn trị bao gồm một véc tơ tái tổ hợp, sao chép thiếu (replication-deficient) có nguồn gốc từ adenovirus của loài tinh tinh (ChAdOx1), được mã hóa gắn protein bề mặt (S glycoprotein/ spike protein) của SARS-CoV-2. Chất sinh miễn dịch SARS-CoV-2 S có trong vắc xin ảnh hưởng tới giai đoạn tiền hợp nhất cấu trúc trimeric (trimeric pre-fusion conformation); trình tự mã hóa không bị thay đổi để ổn định các protein-S (spike protein) trong cấu trúc tiền hợp nhất. Sau khi sử dụng, glycoprotein S của SARS-CoV-2 được phát huy tại chỗ để kích thích kháng thể trung hòa và đáp ứng miễn dịch tế bào, có thể góp phần chống lại COVID-19.
Cơ chế tác dụng (Cho bệnh nhân)
Vaccine AstraZeneca sử dụng vector là virus adeno mất khả năng sao chép của tinh tinh, dựa trên phiên bản suy yếu của virus adeno (virus cúm gây bệnh ở tinh tinh), có chứa vật chất di truyền là protein gai bề mặt của virus gây bệnh COVID-19 được gọi tên là Spike hoặc S. Protein, Spike chính là thành phần tiên phong mở đường tiến công cho virus SARS-CoV-2 xâm nhập cơ thể con người. Đây cũng là mục tiêu tấn công của hệ miễn dịch khi virus SARS-CoV-2 xâm nhập. Sau khi tiêm vắc xin, protein gai bề mặt được sản xuất, các tế bào miễn dịch sẽ ghi nhớ cách chống lại virus SARS-CoV-2 nếu loại virus này tấn công cơ thể trong tương lai.
Hiệu quả lâm sàng
Phân tích dữ liệu tổng hợp từ COV002 và COV003
Hiệu quả lâm sàng của vắc xin phòng ngừa COVID-19 AstraZeneca đã được đánh giá dựa trên phân tích dữ liệu tổng hợp từ hai thử nghiệm ngẫu nhiên, mù đôi, có đối chứng (Vẫn đang tiếp tục nghiên cứu): một nghiên cứu giai đoạn II / III, COV002, ở người lớn ≥18 tuổi (bao gồm người cao tuổi) ở Anh; và một nghiên cứu giai đoạn III, COV003, ở người lớn ≥18 tuổi (kể cả người cao tuổi) ở Brazil. Các nghiên cứu đã loại trừ những người tham gia mắc bệnh tim mạch, tiêu hóa, gan, thận, nội tiết / chuyển hóa nặng và / hoặc không kiểm soát được, và bệnh thần kinh; cũng như những người bị ức chế miễn dịch nghiêm trọng, phụ nữ mang thai và những người tham gia có tiền sử nhiễm SARS-CoV-2. Có thể tiêm vắc xin cúm (influenza vaccine) 7 ngày trước hoặc sau bất kỳ liều nào của Vắc xin phòng ngừa COVID-19 AstraZeneca. Tất cả những người tham gia dự kiến sẽ được theo dõi đến 12 tháng, để đánh giá mức độ an toàn và hiệu quả chống lại dịch COVID-19.
Trong phân tích tổng hợp về hiệu quả, những người tham gia ≥18 tuổi được tiêm hai liều (5 × 10^10 hạt vi-rút mỗi liều tương ứng với không ít hơn 2,5 × 10^8 đơn vị lây nhiễm) của Vắc xin phòng ngừa COVID-19 AstraZeneca (N = 6,106) hoặc đối chứng (vắc-xin viêm não mô cầu hoặc nước muối – giả dược) (N = 6,090), được tiêm qua đường tiêm bắp.
Do những hạn chế bị động, khoảng thời gian giữa liều 1 và liều 2 dao động từ 3 đến 23 tuần (21 đến 159 ngày), với 86,1% người tham gia được tiêm hai liều trong khoảng thời gian từ 4 đến 12 tuần (28 đến 84 ngày).
Nhân khẩu học cơ bản được cân bằng tốt giữa các nhóm vắc xin phòng ngừa COVID-19 AstraZeneca và các nhóm điều trị đối chứng. Trong phân tích tổng hợp, trong số những người tham gia đã được tiêm vắc xin phòng ngừa COVID-19 AstraZeneca với khoảng cách liều từ 4 đến 12 tuần, 87,0% người tham gia từ 18 đến 64 tuổi (13,0% 65 tuổi trở lên và 2,8% 75 tuổi trở lên); 55,1% đối tượng là nữ; 76,2% là người Da trắng, 6,4% người da đen và 3,4% người châu Á. Tổng số 2.068 (39,3%) người tham gia có ít nhất một bệnh đi kèm từ trước (được định nghĩa là BMI ≥30 kg / m2, rối loạn tim mạch, bệnh hô hấp hoặc tiểu đường). Tại thời điểm phân tích, thời gian theo dõi trung bình sau liều 2 là 78 ngày.
Kết quả cuối cùng về các trường hợp mắc COVID-19 được đưa ra bởi một ủy ban độc lập, ủy ban này cũng ấn định mức độ nghiêm trọng của bệnh theo thang tiến triển lâm sàng của WHO. Tổng số 218 người tham gia bị mắc COVID-19 (đã được xác nhận về mặt virus học SARS-CoV-2) trong vòng 15 ngày sau liều thứ hai với ít nhất một triệu chứng COVID-19 (sốt (được định nghĩa là ≥37,8 ° C), ho, khó thở, mất khướu giác , hoặc mất vị giác) và không có bằng chứng về việc nhiễm SARS-CoV-2 trước đó. Vắc xin phòng ngừa COVID-19 AstraZeneca làm giảm đáng kể tỷ lệ mắc bệnh COVID-19 so với đối chứng (xem Bảng 2).
Bảng 2 Hiệu quả của vắc xin phòng ngừa COVID-19 AstraZeneca chống lại COVID-19 (a)
| Dân số | Vắc-xin phòng ngừa covid-19 AstraZeneca | Nhóm đối chứng | Hiệu quả của vắc xin% (95%) CI (b) | ||
| N | Số ca mắc COVID-19 , n (%) | N | Số ca mắc COVID-19 , n (%) | ||
| Chế độ cấp phép | |||||
| 4-12 tuần
(28 đến 84 ngày) |
5,258 | 64 (1,2) | 5,210 | 154 (3,0) | 59,5
(45,8, 69,7) |
N = Tổng số người tham gia trong mỗi nhóm; n = Số người mắc được xác nhận; CI = Khoảng tin cậy;
a Điểm cuối về hiệu quả dựa trên các trường hợp COVID-19 đã được xác nhận ở các đối tượng từ 18 tuổi trở lên có kết quả âm tính lúc ban đầu, những người đã tiêm hai liều và đang nghiên cứu ≥ 15 ngày sau liều thứ hai.
b CI không được điều chỉnh cho sự đa dạng.
Hiệu quả của vắc xin là 62,6% (95% CI : 50,9; 71,5) ở những người tham gia được tiêm hai liều khuyến cáo với bất kỳ khoảng cách liều nào (dao động từ 3 đến 23 tuần), trong một phân tích được chỉ định trước.
Liên quan đến việc nhập viện COVID-19 (Xếp loại mức độ nghiêm trọng của WHO ≥4), có 0 (0,0%; N = 5,258) trường hợp nhập viện COVID-19 ở những người tham gia đã được tiêm hai liều vắc xin phòng ngừa COVID-19 AstraZeneca (≥15 ngày sau liều 2) như so với 8 (0,2%; N = 5,210) ở nhóm đối chứng, bao gồm một trường hợp nặng (Xếp loại mức độ nghiêm trọng của WHO ≥6), được báo cáo ở nhóm đối chứng. Ở tất cả những người tham gia đã được tiêm ít nhất một liều, kể từ 22 ngày sau liều 1, có 0 (0,0%, N = 8,032) trường hợp nhập viện COVID-19 ở những người tham gia đã được tiêm vắc xin phòng ngừa COVID-19 AstraZeneca, so với 14 (0,2%, N = 8,026), bao gồm một trường hợp tử vong, được báo cáo so với nhóm đối chứng.
Những người tham gia có từ một hoặc nhiều bệnh đi kèm có hiệu quả vắc xin là 58,3% [CI 95%: 33,6; 73,9]; 25 (1,2%) so với 60 (2,9%), lần lượt với vắc xin phòng ngừa COVID-19 AstraZeneca (N = 2,068) và nhóm đối chứng (N = 2,040); tương tự như hiệu quả của vắc-xin được quan sát thấy trong dân số chung.
Bằng chứng cho thấy khả năng bảo vệ bắt đầu từ khoảng 3 tuần sau khi tiêm liều vắc xin đầu tiên và kéo dài đến 12 tuần. Liều thứ hai nên được tiêm trong khoảng thời gian từ 4 đến 12 tuần sau liều đầu tiên.
Người già
Trong số những người tham gia từ 56 đến 65 tuổi, 8 trường hợp nhiễm COVID-19 đã được báo cáo ở những người đã được tiêm vắc xin phòng ngừa COVID-19 AstraZeneca (≥15 ngày sau liều 2) so với 9 trường hợp dùng thuốc đối chứng; Có 2 trường hợp nhiễm COVID-19 được báo cáo ở những người tham gia trên 65 tuổi, có dùng vắc xin phòng ngừa COVID-19 AstraZeneca (≥15 ngày sau liều 2) so với 6 người dùng thuốc đối chứng.
Trẻ em
Cơ quan Dược phẩm châu Âu đã cho phép nhà nghiên cứu hoãn nghĩa vụ gửi kết quả nghiên cứu sử dụng Vắc xin phòng ngừa COVID-19 AstraZeneca trên một hoặc nhiều nhóm trẻ em.
Chấp nhận điều kiện (Do trong tình hình dịch bệnh cấp bách)
Sản phẩm thuốc này đã được ủy quyền theo một chương trình gọi là chương trình phê duyệt có điều kiện. Điều này có nghĩa là các bằng chứng khác về sản phẩm này vẫn còn đang được chờ đợi nghiên cứu.
Cơ quan Dược phẩm châu Âu (The European Medicines Agency) sẽ xem xét thông tin mới về sản phẩm thuốc này ít nhất hằng năm và tờ hướng dẫn sử dụng này sẽ được cập nhật khi cần thiết.
Cơ chế tác dụng:
Protein S (spike), một protein nằm trên bề mặt virus SARS-CoV-2 (tác nhân gây bệnh COVID-19), có vai trò quan trọng trong việc giúp virus xâm nhập vào cơ thể con người nhờ khả năng bám gắn đặc hiệu vào một thụ thể (ACE2) có mặt ở nhiều loại tế bào người. Đặc biệt, protein này được hệ miễn dịch của cơ thể nhận diện và kích hoạt các phản ứng miễn dịch, hay nói theo cách khác, protein S chính là kháng nguyên mục tiêu.
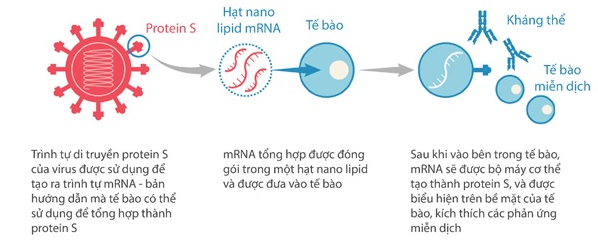
Các vắc xin COVID-19 hiện được phát triển chủ yếu theo hai phương pháp: truyền thống và thế hệ mới. Điểm khác biệt cơ bản của vắc xin thế hệ mới và vắc xin truyền thống là cách kháng nguyên tiếp xúc với hệ miễn dịch của cơ thể. Vắc xin truyền thống chứa virus bị làm yếu hoặc bất hoạt với protein S đã được biểu hiện ở bề mặt virus, hoặc protein S đã được tổng hợp và tinh sạch. Nói cách khác, với phương pháp truyền thống, vắc xin chứa protein S được chế tạo từ bên ngoài, sau đó được đưa vào cơ thể để huấn luyện hệ miễn dịch.
Trong khi đó, vắc xin thế hệ mới chứa các vật liệu di truyền như RNA thông tin (mRNA) hoặc DNA mã hóa của protein S, từ đó sẽ được cơ thể sử dụng và tổng hợp từ bên trong. Cụ thể, sau khi được đưa vào cơ thể, các vật liệu di truyền này sẽ đi vào bên trong tế bào và sử dụng bộ máy của cơ thể để tạo thành protein S, còn mRNA sau đó sẽ bị cơ thể phân hủy. Protein S hoặc các đoạn nhỏ của nó sẽ đi ra ngoài và gắn trên bề mặt tế bào, cho phép hệ thống miễn dịch nhận diện để từ đó kích hoạt các phản ứng chống lại virus khi có virus xâm nhập vào cơ thể. Quan trọng hơn, khi hệ thống miễn dịch được kích hoạt, một loại tế bào miễn dịch được gọi là tế bào B có thể sản xuất ra kháng thể giúp phá hủy cấu trúc của virus hoặc ngăn virus bám gắn vào các tế bào, và tế bào T gây độc tế bào (killer T cells) tiêu diệt các tế bào bị xâm nhiễm bởi virus, để chống lại việc virus nhân lên.
[XEM TẠI ĐÂY]
5.2. Dược động học:
Không áp dụng.
5.3 Giải thích:
Chưa có thông tin. Đang cập nhật.
5.4 Thay thế thuốc :
Chưa có thông tin. Đang cập nhật.
*Lưu ý:
Các thông tin về thuốc trên Pharmog.com chỉ mang tính chất tham khảo Khi dùng thuốc cần tuyệt đối tuân theo theo hướng dẫn của Bác sĩ
Chúng tôi không chịu trách nhiệm về bất cứ hậu quả nào xảy ra do tự ý dùng thuốc dựa theo các thông tin trên Pharmog.com
6. Phần thông tin kèm theo của thuốc:
6.1. Danh mục tá dược:
L-Histidine, L-Histidine hydrochloride monohydrate, Magnesium chloride hexahydrate, Polysorbate 80 (E 433), Ethanol, Sucrose, Natri clorua, Dinatri edetat (dihydrat), Nước cất pha tiêm
6.2. Tương kỵ :
Sản phẩm thuốc này không được trộn lẫn với các sản phẩm thuốc khác hoặc pha loãng.
6.3. Bảo quản:
Lọ chưa mở: 6 tháng khi bảo quản trong tủ lạnh (2 ° C – 8 ° C)
Lọ đã mở: Tính ổn định khi sử dụng về mặt hóa học và vật lý đã được chứng minh từ khi mở lọ (lần đâm kim đầu tiên) đến khi sử dụng không quá 48 giờ trong tủ lạnh (2 ° C – 8 ° C). Trong khoảng thời gian này, sản phẩm có thể được giữ và sử dụng ở nhiệt độ lên đến 30 ° C trong thời gian tối đa 6 giờ. Sau khoảng thời gian này, sản phẩm phải được loại bỏ. KHÔNG ĐƯỢC BỎ LẠI VÀO TỦ LẠNH.
Theo quan điểm vi sinh, sau khi mở nắp lần đầu nên sử dụng vắc xin ngay lập tức. Nếu vắc xin không được sử dụng ngay, người sử dụng phải chịu trách nhiệm về thời gian và điều kiện bảo quản trong thời gian sử dụng.
Các biện pháp phòng ngừa đặc biệt khi bảo quản
Bảo quản trong tủ lạnh (2 ° C – 8 ° C). Không để đóng băng.
Giữ lọ trong thùng carton để tránh ánh sáng.
6.4. Thông tin khác :
Dữ liệu an toàn tiền lâm sàng
Độc tính gen / Khả năng gây ung thư
Cả hai nghiên cứu về độc tính di truyền và khả năng gây ung thư đều không được thực hiện. Các thành phần của vắc-xin không được cho là có khả năng gây độc cho gen.
Độc tính sinh sản
Các nghiên cứu trên động vật về khả năng gây độc đối với sinh sản và phát triển vẫn chưa được hoàn thành.
Một nghiên cứu sơ bộ về độc tính sinh sản trên chuột không cho thấy độc tính ở chuột mẹ hoặc bào thai.
6.5 Tài liệu tham khảo:
Bản dịch từ HDSD Vắc xin.
7. Người đăng tải /Tác giả:
Kiểm duyệt , hiệu đính và đăng tải: PHARMOG TEAM