I. Dùng omega-3 fatty acids hàng ngày cần thiết hay chỉ là thời thượng do quảng cáo ?
Có nhiều ý kiến trái chiều ủng hộ và chống đối việc dùng Omega-3 fatty acids, điều này dễ gây bối rối cho nhiều bạn, ta hãy xem xét chủ đề này dưới khía cạnh pharmacology.
Hình 1.
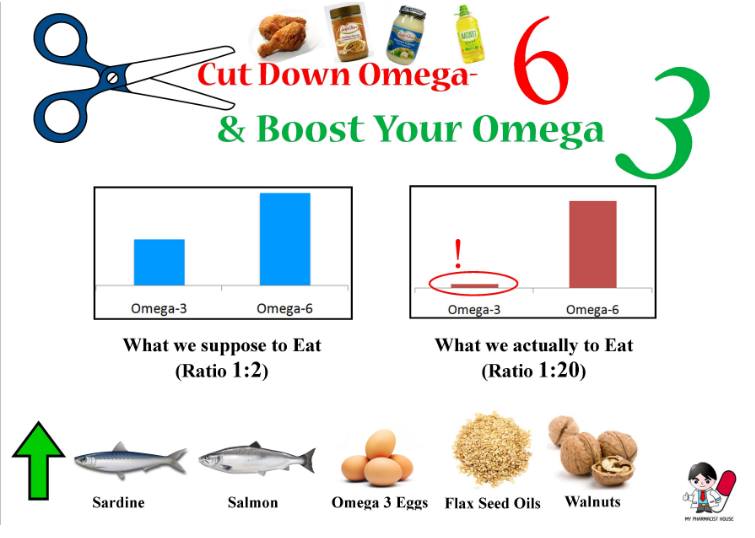
Trước hết kết quả nghiên cứu về dinh dưỡng có một phát hiện khá bất ngờ (2009) (hình 1) theo đó người ta giả định rằng tỷ lệ trong khẩu phần hàng ngày giữa omega-3 và omega-6 là 1/2 nhưng phân tích thực tế cho thấy tỷ lệ này chỉ là 1/20, số liệu này bắt buộc người ta phải thừa nhận cần thiết phải dùng omega-3 bổ sung (hình 2) để ngăn chận những phản ứng viêm quá phát.
Hình 2.
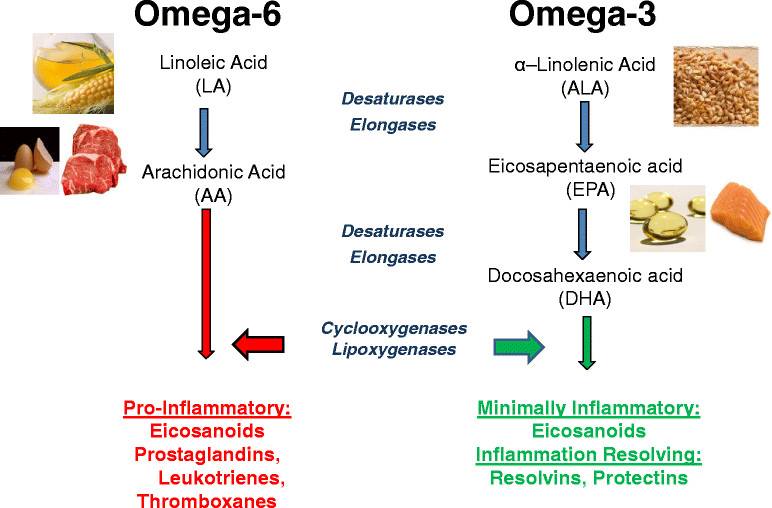
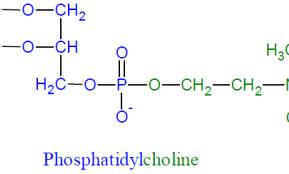
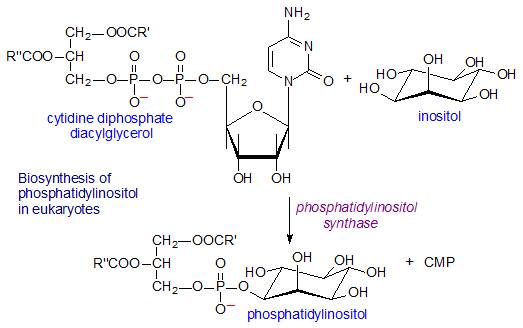
Chúng ta cũng không lạ gì rằng phản ứng viêm nếu xảy ra có nguồn gốc từ phosphatidylcholine & phosphatidylinositol của màng bào tương dưới tác động thủy phân của Phospholipase A2 mà vị trí phân cắt của nó xảy ở C2 của glycerol (hình 3&4)
Hình 3.
Hình 4.
Ở đây là sự hiện hữu của arachidonic acid điều xảy ra sau đó chẳng làm ai ngạc nhiên cả (hình 5).
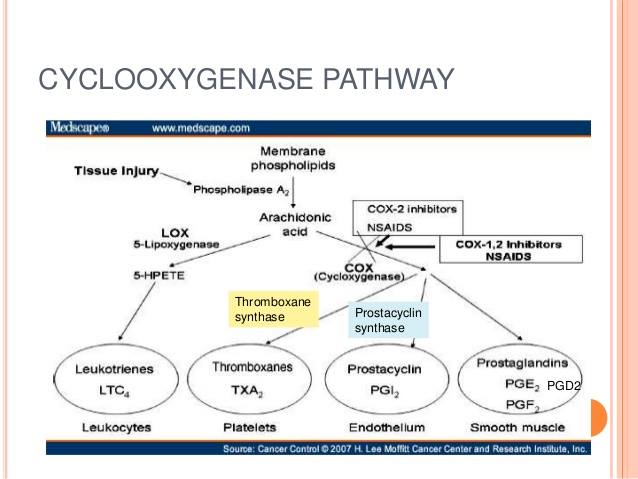
Hình 5.
Chúng cũng chẳng lạ gì cấu trúc của màng bào tương với các phophatidic acids (hình 6), sự điều tiết của phosphatidylcholine & phosphatidylinositol do các enzymes quen thuộc (hình 7).

Hình 6.
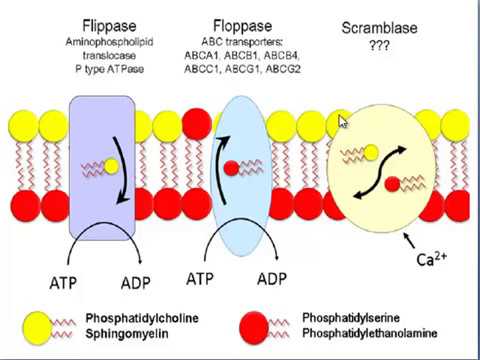
Hình 7.
Sử dụng omega-3 fatty acids chỉ nhằm tăng tỷ lệ hiện hữu ở C2 trên 2 phân tử phosphatidylcholine & phosphatidylinositol (hình 2) điều này sẽ hạn chế hình thành những prostanoids gây hại như PGE2, PGF2 alpha và TBXA2 (hình 5).
Như vậy vấn đề đã quá rõ ràng không có gì phải tranh cãi nữa.
II. Vậy có nên dùng omega 3 hay không ? Có liên hệ gì với Ung thư và Alzheimer ?
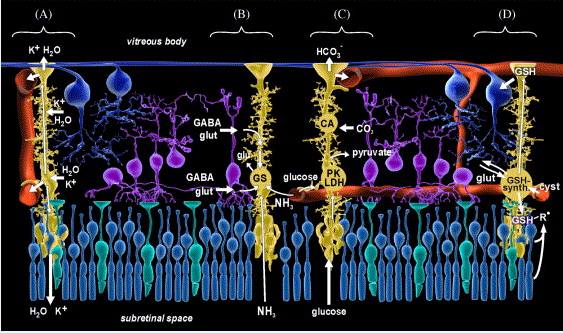
Trước hết hãy xem cấu trúc của blood – brain barrier (Hình 1) và võng mạc (Hình 2) ta sẽ thấy điểm chung đó là Astrocyte và Muller cell đều là tế bào đệm ở giữa mô thần kinh, điều quan trọng hơn là những tế bào đệm (glial cell) này là nguồn cung cấp dinh dưỡng chính cho các loại neuron hay tế bào nón và tế bào que, tế bào hạch trung gian của võng mạc.

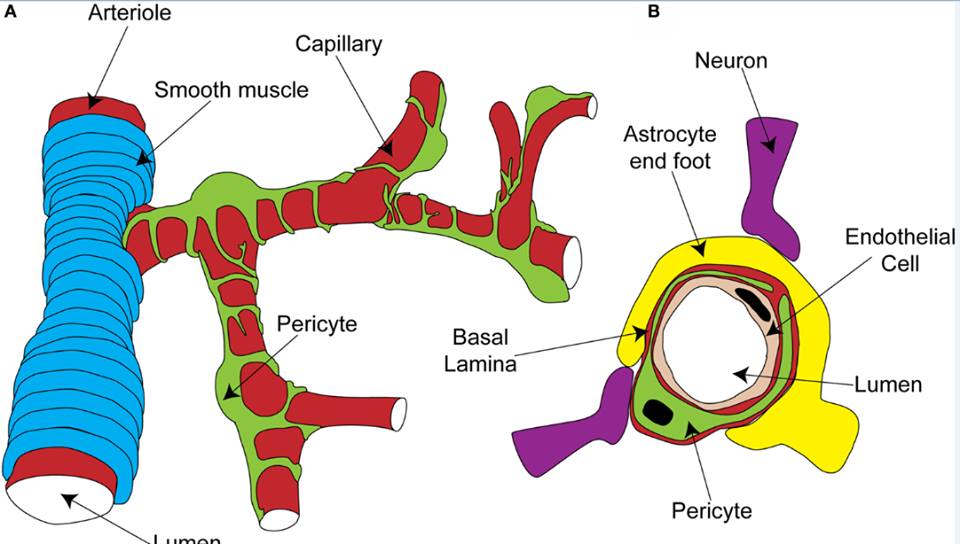
Chung quanh các tế bào nội mạc (Endothelium) của vi quản còn có những pericytes (Hình 3) tạo nối kết chặt (tight junction) với một bên là tế bào đệm một bên khác là tế bào nội mạc của mạch máu, pericytes là cơ chế làm co hoặc giãn mao mạch thông qua tín hiệu thần kinh và các chất hóa học vận mạch.
Từ lâu người ta đã biết sự giảm hoạt của pericytes là nguồn gốc của nhiều bệnh lý như đột quỵ , Alzheimer và bệnh lý võng mạc kể cả do tiểu đường. Các tight junction gồm những protein được gọi là Cadherin (calcium dependant adhesion) (Hình 4), nối kết giữa tế bào ngoại mạch với mạch máu là VE-cadherin (vascular endothelial cadherin) và giữa tế bào ngoại mạch với tế bào thần kinh đệm là N-cadherin (neural cadherin). Cadherin được nối kết với PS1 (presenilin 1) và beta hay gamma catenin để từ đó nối kết gián tiếp với alpha catenin gắn vào sợi actin (cytoskeleton) , tất cả các nối kết này đều là nối yếu (nối hydrogen).
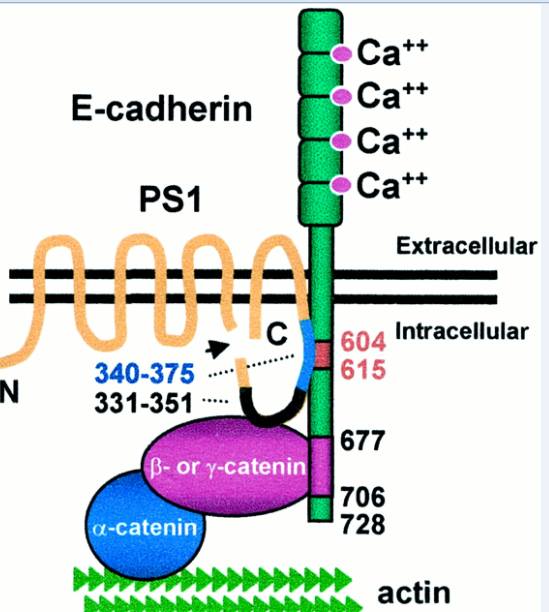
Cadherin trên màng nội mô mạch máu hay tế bào ngoại mạch đều nằm trong lipid raft (Hình 5), được giới hạn và giữ chặt với các phospholipids màng khác bởi cholesterol và glycosphingolipids. Presenilin 1 là một protein bậc III thành phần của một cleavage molecule khi được lắp ghép với các phân tử khác tạo thành beta secretase cắt một protein có tên là APP (amyloid precuser protein) tạo thành beta amyloid nổi tiếng trong bệnh Alzheimer nhưng ở đây presenilin 1 chỉ là một phân tử đơn độc và chức năng chỉ là cố định cadherin trên màng (Hình 6).
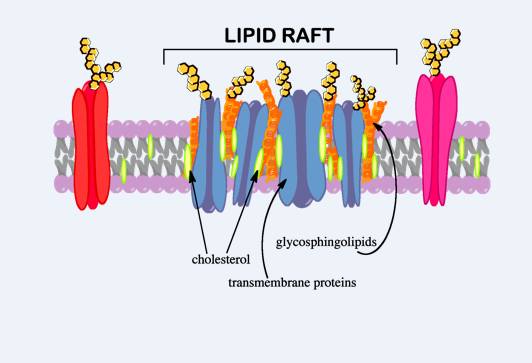
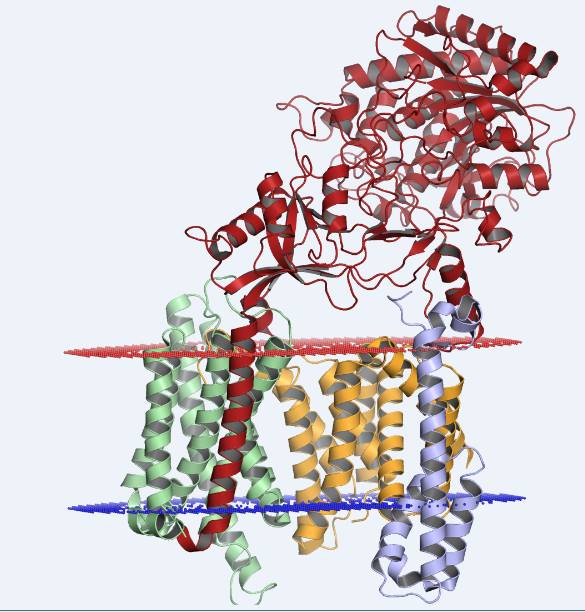
Hình 6 cho thấy một phân tử betasecretase với các thành phần đỏ: Nicastrin, xanh lá: Pen2. lam: APH1 cam: presenilin1.
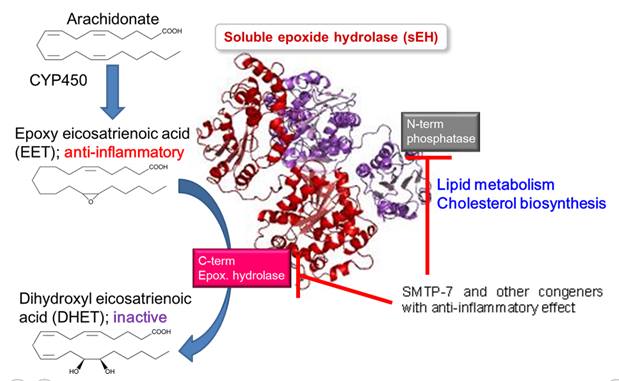
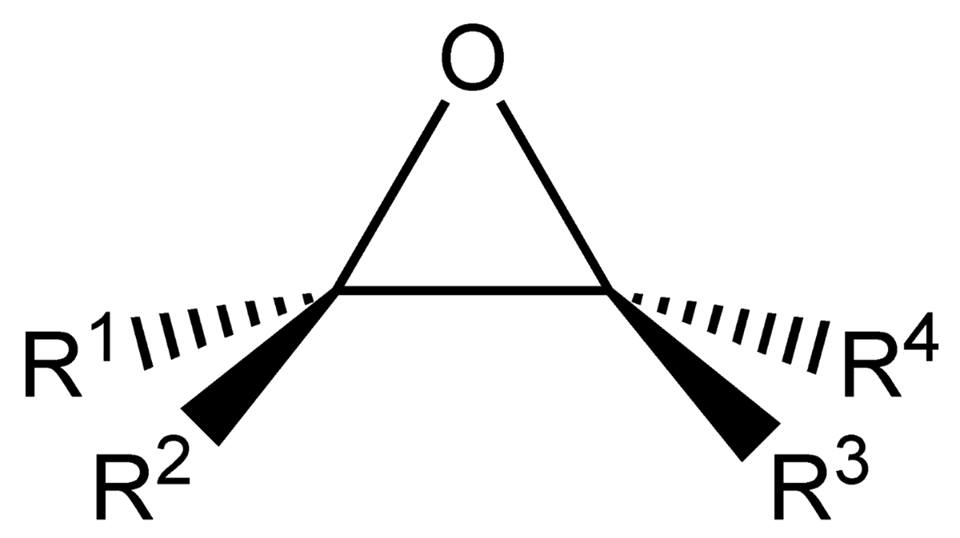
Vấn đề then chốt của bài viết này là overexpression của sEH ( soluble epoxide hydrolase) (Hình 7), một men chuyển hóa DHA (docosahexaenoic acid), một acid béo không bão hòa gọi là omega 3 fatty acid, khi DHA được chuyển vận vào tế bào nội mạc của mạch máu sẽ được biến thành epoxide (Hình 8) – một phân tử ether tricyclic. Đó là một phân tử acid béo dễ bị bẻ gãy, sEH sẽ chuyển hóa epoxide thành 19,20- dihydroxydocosapentaenoic acid. 19,20 DHDP chính là một phân tử tín hiệu gây tan rã nối kết giữa presenilin 1 và cadherin làm cadherin không trụ được trên màng tế bào nội mô của mạch máu (Hình 9).
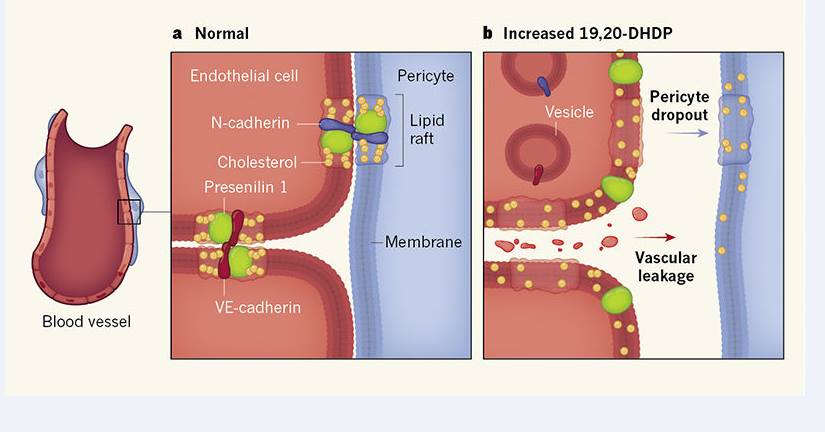
Hậu quả của hiện tượng này là phá vỡ tight junction khiến cho huyết tương và cả Vascular endothilial growth factor ( VEGF) đi vào extracellular matrix làm tăng sinh mạch máu angiogenesis các mạch máu tân tạo này rất dễ vỡ gây viêm và phù võng mạc.
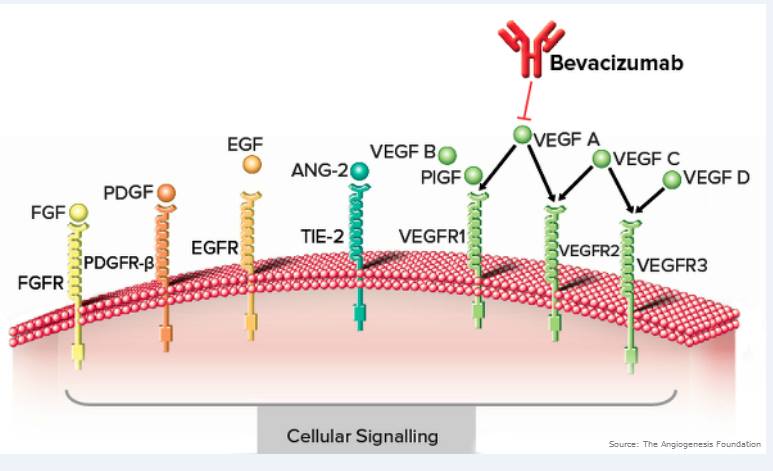
Hiện tượng này cũng thấy trong các solid tumor ác tính vì vậy người ta đã dùng Bevacizumab trong cả ung thư lẫn bệnh lý võng mạc, trong bệnh lý võng mạc điều trị này không hiệu quả lắm vì vậy người ta nghi ngờ rằng còn có thể hiện hữu một cơ chế bệnh sinh nào khác nữa và hôm nay Hu et al hé mở cho chúng ta một con đường chuyển hóa khác có thể là mục tiêu điều trị khác? Nên nhớ đây chỉ là một thực nghiệm trên chuột liệu con đường chuyển hóa này có hiện hữu trên con người?
Theo BS.Phùng Trung Hùng


