1. Tên hoạt chất và biệt dược:
Hoạt chất : Ceftazidime
Phân loại: Thuốc Kháng sinh nhóm cephalosporin thế hệ 3.
Nhóm pháp lý: Thuốc kê đơn ETC – (Ethical drugs, prescription drugs, Prescription only medicine)
Mã ATC (Anatomical Therapeutic Chemical): J01DD02.
Biệt dược gốc: FORTUM
Biệt dược: Sitacef
Hãng sản xuất : Laboratorio Internacional Argentino S.A
2. Dạng bào chế – Hàm lượng:
Dạng thuốc và hàm lượng
Lọ 1 g, bột vô khuấn để pha tiêm hoặc tiêm truyền.
Hàm lượng và liều lượng biểu thị theo dạng ceftazidim khan: 1 g ceftazidim khan tương ứng với 1,16 g ceftazidim pentahydrat.
Thuốc tham khảo:
| SITACEF 1g | ||
| Mỗi lọ thuốc bột pha tiêm có chứa: | ||
| Ceftazidime Natri | …………………………. | 1000 mg |
| Tá dược | …………………………. | vừa đủ (Xem mục 6.1) |

3. Video by Pharmog:
[VIDEO DƯỢC LÝ]
————————————————
► Kịch Bản: PharmogTeam
► Youtube: https://www.youtube.com/c/pharmog
► Facebook: https://www.facebook.com/pharmog/
► Group : Hội những người mê dược lý
► Instagram : https://www.instagram.com/pharmogvn/
► Website: pharmog.com
4. Ứng dụng lâm sàng:
4.1. Chỉ định:
Sitacef được chỉ định để điều trị các bệnh nhiễm trùng dưới đây ở người lớn và trẻ em bao gồm cả trẻ sơ sinh (từ khi sinh ra):
Viêm phổi bệnh viện.
Nhiễm trùng phế quản-phổi ở bệnh nhân xơ nang.
Viêm màng não do vi khuẩn.
Viêm tai giữa mạn tính.
Viêm tai ngoài ác tính.
Nhiễm trùng đường tiết niệu có biến chứng.
Nhiễm trùng da và mô mềm có biến chứng.
Nhiễm trùng trong ổ bụng có biến chứng.
Nhiễm trùng xương và khớp.
Nhiễm trùng phúc mạc kết hợp với thẩm phân phúc mạc ở bệnh nhân thẩm phân phúc mạc liên tục.
Điều trị ở bệnh nhân nhiễm trùng máu xảy ra kết hợp với hoặc bị nghi ngờ liên quan đến bất kỳ các nhiễm trùng được liệt kê như trên.
Ceftazidim được sử dụng ở bệnh nhân bị sốt kèm giảm bạch cầu trung tính bị nghi ngờ do nhiễm khuẩn.
Ceftazidim có thể được sử dụng trong dự phòng nhiễm trùng đường tiết niệu ở bệnh nhân phẫu thuật cắt tuyến tiền liệt qua niệu đạo (TURP).
Việc lựa chọn kháng sinh ceftazidim nên cân tính tới phổ kháng khuẩn của kháng sinh mà thường chủ yếu giói hạn với các vi khuẩn Gram (-) kị khí.
Ceftazidim nên được dùng đồng thời với các kháng sinh khác bất kỳ khi nào mà phạm vi hoạt động của vi khuẩn không ở trong phổ hoạt động của kháng sinh.
Cân nhắc thực hành theo các hướng dẫn chính thức để sử dụng kháng sinh đúng
4.2. Liều dùng – Cách dùng:
Cách dùng :
dùng tiêm bắp sâu, tiêm tĩnh mạch chậm trong 3 – 5 phút, hoặc tiêm truyền tĩnh mạch.
Tiêm bắp: Hoà tan thuốc bằng 4ml nước cất pha tiêm (250 mg/ml). Dung dịch sau khi pha nên dùng ngay hoặc trong vòng 18 giờ ở nhiệt độ phòng hoặc 7 ngày khi để tủ lạnh.
Tiêm tĩnh mạch, tiêm truyền tĩnh mạch: Hoà tan thuốc tương ứng với 10ml và 100ml nước cất pha tiêm, dung dịch natri clorid 0,9%, hoặc dextrose 5%. Dung dịch sau khi pha được dùng ngay hoặc trong vòng 24 giờ ở nhiệt độ phòng hoặc 7 ngày khi để tủ lạnh.
Liều dùng:
Người lớn và trẻ em ≥ 40 kg:
| Phương pháp sử dụng gián đoạn | |
| Loại nhiễm trùng | Liều điều trị |
| Nhiễm trùng phế quản-phổi ở bệnh nhân xơ nang | 100 – 150 mg/kg/ngày mỗi 8 h, tối đa 9 h mỗi ngày (1) |
| Giảm bạch cầu trung tính do sốt | 2 g mỗi 8 h |
| Viêm phổi bệnh viện | |
| Viêm màng não do vi khuẩn | |
| Nhiễm khuẩn huyết * | |
| Nhiễm trùng xương và khớp | 1 – 2 g mỗi 8 h |
| Nhiễm trùng da và mô mềm có biến chứng | |
| Nhiễm trùng trong ổ bụng có biến chứng | |
| Nhiễm trùng phúc mạc kết hợp với thẩm phân phúc mạc ở bệnh nhân thẩm phân phúc mạc liên tục | |
| Nhiễm khuẩn đường tiết niệu có biến chứng | 1 – 2 g mỗi 8 h hoặc 12 h |
| Dự phòng trong phẫu thuật cắt tuyến tiền liệt qua niệu đạo (TURP) | 1 g lúc gây mê và liều thứ 2 lúc bỏ ống thông |
| Viêm tai giữa mãn tính. | 1 – 2 g mỗi 8 h |
| Viêm tai ngoài ác tính. | |
| Phương pháp truyền liên tục | |
| Loại nhiễm trùng | Liều dùng |
| Giảm bạch cầu trung tính do sốt | Liều tải 2 g, sau đó truyền liên tục 4 – 6 g mỗi 24 h (1) |
| Viêm phổi bệnh viện | |
| Nhiễm trùng phế quản-phổi ở bệnh nhân xơ nang | |
| Viêm màng não do vi khuẩn | |
| Nhiễm khuẩn huyết * | |
| Nhiễm trùng xương và khớp | |
| Nhiễm trùng da và mô mềm có biến chứng | |
| Nhiễm trùng trong ổ bụng có biến chứng | |
| Nhiễm trùng phúc mạc kết hợp với thẩm phân phúc mạc ở bệnh nhân thẩm phân phúc mạc liên tục |
(1): Ở người lớn với chức năng thận bình thường, liều 9 g/ngày được sử dụng mà không có tác dụng phụ.
*: Khi kết hợp với hoặc nghi ngờ liên quan đến các nhiễm trùng được liệt kê ở mục “Chỉ định”
Trẻ em < 40kg:
| 2.1 Với trẻ sơ sinh và trẻ mới biết đi > 2 tháng và trẻ em < 40 kg. | |
| Loại nhiễm trùng | Liều dùng |
| Phương pháp sử dụng gián đoạn | |
| Nhiễm khuẩn đường tiết niệu có biến chứng | 100 – 150 mg/kg/ngày, chia làm 3 lần, tối đa 6 g/ngày. |
| Viêm tai giữa mãn tính. | |
| Viêm tai ngoài ác tính. | |
| Trẻ em bị giảm bạch cầu trung tính | 150 mg/kg/ngày, chia làm 3 lần, tối đa 6 g/ngày. |
| Nhiễm trùng phế quản-phổi ở bệnh nhân xơ nang | |
| Viêm màng não do vi khuẩn | |
| Nhiễm khuẩn huyết * | |
| Nhiễm trùng xương và khớp | 100 – 150 mg/kg/ngày, chia làm 3 lần, tối đa 6 g/ngày. |
| Nhiễm trùng da và mô mềm có biến chứng | |
| Nhiễm trùng trong ổ bụng có biến chứng | |
| Nhiễm trùng phúc mạc kết hợp với thẩm phân phúc mạc ở bệnh nhân thẩm phân phúc mạc liên tục | |
| Phương pháp truyền liên tục | |
| Giảm bạch cầu trung tính do sốt | Liều tải 60 – 100 mg/kg, sau đó truyền liên tục 100 – 200 mg/kg/ngày, tối đa 6 g/ngày |
| Viêm phổi bệnh viện | |
| Nhiễm trùng phế quản-phổi ở bệnh nhân xơ nang | |
| Viêm màng não do vi khuẩn | |
| Nhiễm khuẩn huyết * | |
| Nhiễm trùng xương và khớp | |
| Nhiễm trùng da và mô mềm có biến chứng | |
| Nhiễm trùng trong ổ bụng có biến chứng | |
| Nhiễm trùng phúc mạc kết hợp với thẩm phân phúc mạc ở bệnh nhân thẩm phân phúc mạc liên tục |
Trẻ sơ sinh và trẻ em < 2 tháng
Dùng gián đoạn:
Hầu hết các nhiễm trùng : 25 – 60 mg/kg/ngày chia làm 2 lần(1)
(1): Trẻ sơ sinh và trẻ < 2 tháng, thời gian bán thải trong huyết thanh có thể cao hơn 3 – 4 lần so với người lớn.
*: Khi kết hợp với hoặc nghi ngờ liên quan đến các nhiễm trùng được liệt kê ở mục “Chỉ định”.
Đối tượng trẻ em : Hiệu quả và an toàn của ceftazidim khi truyền liên tục ỏ’ trẻ sơ sinh và trẻ em < 2 tháng vẫn chưa được thiết lập.
Người cao tuổi: theo quan điểm về tuổi tác liên quan đến việc giảm độ thanh thải của ceftazidim ở người cao tuổi, liều dùng không nên vượt quá 3 g ở bệnh nhân trên 80 tuổi.
Bệnh nhân suy giảm chức năng thận : ceftazidim được đào thải qua thận dưới dạng không đổi. Vì vậy, cần phải giảm liều ở bệnh nhân suy thận.
Liều tải đầu tiên là 1 g. Liều duy trì nên dựa trên độ thanh thải creatinin
Liều duy trì được khuyến cáo ở bệnh nhân suy thận – phương pháp truyền gián đoạn:
Với người lớn và trẻ em ≥ 40 kg
| Độ thanh thải creatinin (ml/phút) | Creatinin huyết tương (µmol/l) | Liều duy trì |
| 50 – 31 | 150 – 200 | 1 g cách 12 giờ 1 lần |
| 30 – 16 | 200 – 350 | 1 g cách 24 giờ 1 lần |
| 15 – 6 | 350 – 500 | 0,5 g cách 24 giờ 1 lần |
| < 5 | > 500 | 0,5 g cách 48 giờ 1 lần |
Ở bệnh nhân bị nhiễm trùng nặng: nên tăng 50% đơn vị liều hoặc tăng tần suất sử dụng. Trẻ em với độ thanh thải creatinin nên được điều chỉnh theo diện tích bề mặt cơ thể hoặc trọng lượng nạc cơ thể.
Trẻ em < 40 kg.
| Độ thanh thải creatinin (ml/phút)** | Creatinin huyết tương *µmol/l | Liều dùng |
| 50 – 31 | 150 – 200 | 25 mg/kg cách 12 giờ 1 lần |
| 30 – 16 | 200 – 350 | 25 mg/kg cách 24 giờ 1 lần |
| 15 – 6 | 350 – 500 | 12,5 mg/kg cách 24 giờ 1 lần |
| < 5 | > 500 | 12,5 mg/kg cách 48 giờ 1 lần |
| * Các giá trị creatinin huyết thanh là các giá trị hướng dẫn, có thể không chỉ ra chính xác mức độ giảm giống nhau đối với tất cả các bệnh nhân bị suy thận. ** Ước tính dựa trên diện tích bề mặt cơ thể hoặc được đo. |
||
Cần phải theo dõi lâm sàng chặt chẽ về độ an toàn và hiệu quả.
Liều duy trì được khuyến cáo của ceftazidim ở bệnh nhân suy thận – phương pháp truyền liên tục:
Người lớn và trẻ em ≥ 40 kg:
| Độ thanh thải creatinin (ml/phút) | Creatinin huyết tương µmol/l | Liều dùng |
| 50 – 31 | 150 – 200 | Liều tải 2 g, sau đó dùng 1 – 3 g/24 h |
| 30 – 16 | 200 – 350 | Liều tải 2 g, sau đó dùng 1 g/24h |
| ≤ 15 | > 350 | Chưa được xác định |
Cần phải theo dõi lâm sàng chặt chẽ về độ an toàn và hiệu quả.
Trẻ em < 40 kg: Độ an toàn và hiệu quả khi dùng đường truyền tĩnh mạch liên tục cho trẻ em bị suy thận < 40 kg chưa được thiết lập. Cần theo dõi lâm sàng chặt chẽ về độ an toàn và hiệu quả. Nếu dùng đường truyền tĩnh mạch liên tục cho trẻ em bị suy thận, độ thanh thải creatinin nên được điều chỉnh so với diện tích bề mặt cơ thể hoặc trọng lượng nạc cơ thể.
Thẩm tách máu:
Thời gian bán thải trong quá trình thẩm tách máu khoảng 3 – 5 h. Sau mỗi giai đoạn thẩm tách máu, liều duy trì của ceftazidim nên được lặp lại theo bảng bên dưới.
Thẩm phân phúc mạc:
Ceftazidim có thể được sử dụng trong thẩm phân phúc mạc và thẩm phân phúc mạc liên tục ngoại trú (CAPD).
Ngoài việc sử dụng đường truyền tĩnh mạch, ceftazidim có thể được kết hợp vào dịch thẩm tách (thông thường 125 – 250 mg trong 2 lít dịch thẩm tách).
Đối với bệnh nhân bị suy thận đang được thẩm tách máu liên tục động – tĩnh mạch hoặc lọc máu qua màng lọc high-flux trong các đơn vị điều trị chuyên sâu: 1 g mỗi ngày, dùng liều đơn hoặc dùng nhiều lần. Đối với lọc máu qua màng lọc low-flux, theo liều khuyến cáo dùng ở bệnh nhân suy thận.
Đối với bệnh nhân đang lọc máu tĩnh mạch – tĩnh mạch và thẩm tách máu tĩnh mạch – tĩnh mạch, theo liều khuyến cáo theo bàng dưới đây:
Bảng 1: Hướng dẫn liều trong lọc máu liên tục tĩnh mạch – tĩnh mạch
| Độ thanh thải creatinin (ml/phút) | Liều duy trì (mg) tương ứng với tốc độ lọc máu (ml/phút) (liều được sử dụng mỗi 12 h) | |||
| 0 | 5 | 16,7 | 33,3 | 50 |
| 5 | 250 | 250 | 500 | 500 |
| 10 | 250 | 250 | 500 | 500 |
| 15 | 250 | 500 | 500 | 750 |
| 20 | 250 | 500 | 500 | 750 |
| 20 | 500 | 500 | 500 | 750 |
Bảng 2: Hướng dẫn liều trong thẩm tách máu liên tục tĩnh mạch – tĩnh mạch:
| Độ thanh thải creatinin (ml/phút) | Liều duy trì (mg) đối với thẩm tách máu theo tốc độ chảy tương ứng (liều được sử dụng mỗi 12 h) | |||||
| 1 L/h | 2 L/h | |||||
| Tốc độ lọc (L/h) | Tốc độ lọc (L/h) | |||||
| 0,5 | 1 | 2 | 0,5 | 1 | 2 | |
| 0 | 500 | 500 | 500 | 500 | 500 | 750 |
| 5 | 500 | 500 | 750 | 500 | 500 | 750 |
| 10 | 500 | 500 | 750 | 500 | 750 | 1000 |
| 15 | 500 | 750 | 750 | 750 | 750 | 1000 |
| 20 | 750 | 750 | 1000 | 750 | 750 | 1000 |
4.3. Chống chỉ định:
Ngưòi mân cảm với ceftazidim, bất kỳ kháng sinh nào nhóm penicilin và cephalosporin hoăc tá dươc của thuốc.
Bệnh nhân có tiền sử quá mẫn nặng (như phản ứng phản vệ) với bất kỳ kháng sinh beta-lactam nào (penicillin, monobactam và carbapenem)
4.4 Thận trọng:
Quá mẫn:
Giống như tất cả các thuốc kháng khuẩn nhóm beta-lactam, phản ứng quá mẫn nghiêm trọng hoặc đôi khi gây tử vong đã được báo cáo. Trường hợp xảy ra các phản ứng quá mẫn nghiêm trọng, ngừng điều trị ngay lập tức với ceftazidim và tiến hành các biện pháp cấp cứu đầy đủ.
Trước khi bắt đầu điều trị, nên hỏi kỹ bệnh nhân về tiền sử các phản ứng quá mẫn với ceftazidim, với các kháng sinh nhóm cephalosporin hoặc với các kháng sinh nhóm beta-lactam. Thận trọng khi sử dụng cho bệnh nhân có tiền sử xảy ra các phản ứng quá mẫn không nghiêm trọng với bất kỳ các thuốc nhóm beta-lactam khác.
Phổ tác dụng:
Ceftazidim có phổ kháng khuẩn hạn chế. Thuốc không thích hợp sử dụng đơn độc để điều trị nhiễm trùng trừ khi mầm bệnh đã được ghi nhận và được biết đến là nhạy cảm với ceftazidim hoặc có nghi ngờ cao rằng hầu hết các mầm bệnh thích hợp để điều trị với ceftazidim. Điều đặc biệt này áp dụng khi xem xét điều trị cho bệnh nhân bị nhiễm khuẩn huyết, viêm màng não do vi khuẩn, nhiễm trùng da, mô mềm và nhiễm trùng xương, khớp. Ngoài ra, ceftazidim dễ bị thủy phân bởi các beta-lactamase phổ rộng (ESBLs). Do đó, các thông tin về tỷ lệ các vi sinh vật sản xuất ESBLs nên được lưu ý khi lựa chọn ceftazidim để điều trị.
Viêm kết ruôt giả mac
Viêm đại tràng và viêm đại tràng giả mạc do vi khuẩn đã được báo cáo với hầu hết các thuốc kháng khuẩn, bao gồm cả ceftazidim và có thể xảy ra với mức độ nhẹ đến đe dọa tính mạng. Do đó, cần phải xem xét trường hợp này ở những bệnh nhân có biểu hiện tiêu chảy trong hoặc sau khi điều trị với ceftazidim. Cần xem xét ngưng điều trị với ceftazidim và tiến hành các biện pháp điều trị đặc hiệu với Clostridium difficile. Không nên dùng các thuốc ức chế nhu động ruột.
Chức năng thận:
Điều trị đồng thời liều cao các cephalosporin và thuốc gây độc thận như aminoglycosid hoặc thuốc lợi tiểu tác dụng mạnh (như furosemid) có thể ảnh hưởng nghiêm trọng chức năng thận
Ceftazidim được đào thải qua thận, do đó nên giảm liều tùy theo mức độ suy thận. Cần theo dõi chặt chẽ tính an toàn và hiệu quả ở bệnh nhân suy thận. Biến chứng thần kinh đôi khi được báo cáo khi liều dùng không được giảm ở những bệnh nhân bị suy thận.
Sự phát triển quá mức ở các vi sinh vật không nhạy cảm:
Sử dụng kéo dài có thể dẫn đến sự phát triển quá mức của các chủng vi sinh vật không nhạy cảm (như Enterococci, nấm). Điều này có thể phải ngừng điều trị hoặc tiến hành các biện pháp thích hợp khác. Đánh giá lặp lại tình trạng của bệnh nhân là cần thiết.
Các tác động trẽn xét nghiêm và đinh lượng:
Ceftazidim không ảnh hưởng đến các xét nghiệm glucose niệu bằng enzym nhưng có thể có phản ứng dương tính giả với các xét nghiệm bằng phương pháp khử đồng (dung dịch Benedict, dung dịch Fehling, viên Clinitest).
Ceftazidim không ảnh hưởng đến định lượng creatinin bằng picrat kiềm.
Ceftazidim có thể gây dương tính giả với phép thử Coomb ở khoảng 5% bệnh nhân.
Thuốc có chứa Natri
Sitacef lg có chứa 118mg Natri carbonat khan.
Vì vậy nên cân nhấc khi sử dụng trên các bệnh nhân với chế độ ăn kiểm soát muối.
Tác động của thuốc trên người lái xe và vận hành máy móc.
Chưa có nghiên cứu nào về ảnh hưởng của ceftazidim trên khả năng lái xe, vận hành máy. Tuy nhiên, có thế xảy ra tác dụng không mong muốn như chóng mặt gây ảnh hưởng đên khả năng lái xe hoặc vận hành máy móc.
4.5 Sử dụng cho phụ nữ có thai và cho con bú:
Xếp hạng cảnh báo
AU TGA pregnancy category: B1
US FDA pregnancy category: B
Thời kỳ mang thai:
Có rất ít dữ liệu về việc sử dụng ceftazidim trên phụ nũ’ có thai. Các nghiên cứu trên động vật không thấy các tác dụng có hại trực tiếp hoặc gián tiếp trên phụ nữ có thai, sự phát triển của thai nhi/bào thai, quá trình sinh và sau sinh (xem phần dữ liệu tiền lãm sàng).
Chỉ sử dụng ceftazidim cho phụ nữ có thai khi cân nhắc thấy lợi ích nhiều hơn nguy cơ
Thời kỳ cho con bú:
Ceftazidim được bài tiết qua sữa mẹ với lượng nhỏ nhưng không có ảnh hưởng đến trẻ bú mẹ ỏ’ liều điều trị. Do vậy, có thể dùng ceftazidim trong thời gian cho con bú.
Khả năng sinh sản
Không có dữ liệu
4.6 Tác dụng không mong muốn (ADR):
Tác dụng không mong muốn thường gặp: tăng bạch cầu, tăng tiểu cầu, viêm tĩnh mạch hoặc viêm tắc tĩnh mạch khi dùng đường tĩnh mạch, tiêu chảy, tăng enzyme gan tạm thời, ban dát hoặc ban mê đay, đau và/hoặc viêm sau khi tiêm bắp và test Comb dương tính.
Dữ liệu từ các nghiên cứu lâm sàng được tài trợ và không được tài trợ cho thấy tần suất thường gặp và không thường gặp của các tác dụng không mong muốn:
Thường gặp: ≥ 1/100 đến < 1/10.
Ít gặp: ≥ 1/1.000 đến < 1/100.
Hiếm gặp: ≥ 1/10.000 đến < 1/1.000.
Rất hiếm gặp: < 1/10.000.
Không biết đến: không ước tính từ dữ liệu có sẵn.
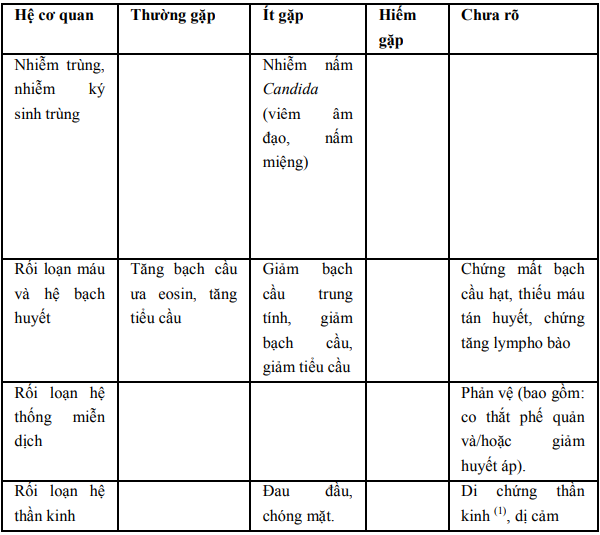
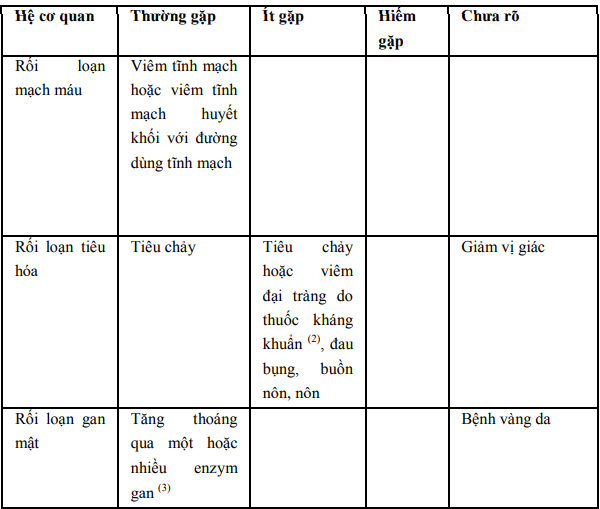
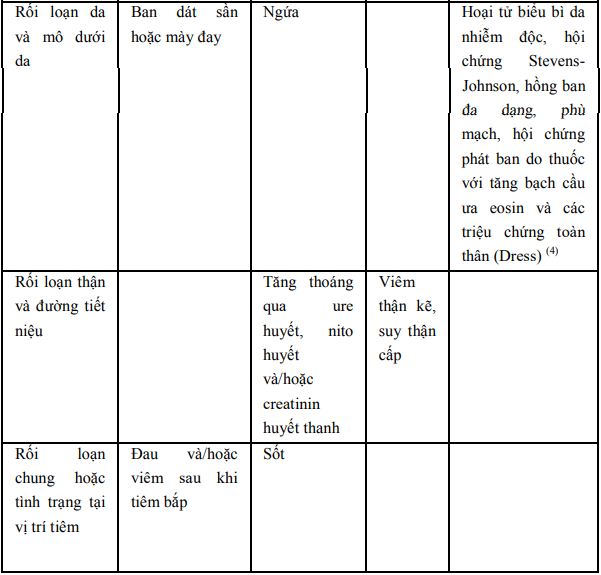
Ghi chú:
(1): Đã có báo cáo về di chứng thần kinh gồm: run, chứng giật run cơ, co giật, bệnh não và hôn mê ở bệnh nhân suy thận mà liều dùng của ceftazidim không được giảm thích hợp.
(2): Tiêu chảy và viêm đại tràng do Clostridium difficile và có thể xảy ra viêm đại tràng giả mạc.
(3): ALT (SGPT), AST (SOGT), LDH, GGT, phosphatase kiềm.
(4): Hiếm có báo cáo hội chứng Dress liên quan đến ceftazidim.
(5): Thử nghiệm Coomb dương tính có thể xảy ra ở khoảng 5% bệnh nhân và có thể can thiệp với phản ứng chéo trong máu.
Thông báo cho Bác sĩ những tác dụng không mong muốn gặp phải khi sử dụng thuốc.
4.7 Hướng dẫn cách xử trí ADR:
Ngừng sử dụng thuốc. Với các phản ứng bất lợi nhẹ, thường chỉ cần ngừng thuốc. Trường hợp mẫn cảm nặng hoặc phản ứng dị ứng, cần tiến hành điều trị hỗ trợ (giữ thoáng khí và dùng epinephrin, thở oxygen, dùng kháng histamin, corticoid…).
4.8 Tương tác với các thuốc khác:
Các nghiên cứu về tương tác thuốc mới chỉ thực hiện với probenecid và furosemide.
Sử dụng đồng thòi cefitazidim với liều cao các thuốc gây độc thận có thể gây hại cho chức năng thận (xem phần Cảnh báo và thận trọng).
Chloramphenicol đối vận với ceftazidim và các kháng sinh cephalosporin khác trên in vitro. Sự liên quan lâm sàng của hiện tượng này vẫn chưa giải thích, nhưng nếu dùng đồng thời ceftazidim và chloramphenicol thì nên cân nhắc tới khả năng xảy ra tương tác đối vận.
Ceftazidim có thể làm giảm hấp thu thuốc tránh thai đường uống.
4.9 Quá liều và xử trí:
Quá liều có thể dẫn đến di chứng thần kinh bao gồm bệnh não, co giật và hôn mê.
Các triệu chứng của quá liều có thể xảy ra nếu các liều không được giảm một cách thích hợp ỏ’ những bệnh nhân suy thận (xem phần 4.2 và 4.4).
Nồng độ ceftazidime có thể được giảm bằng cách thẩm phân máu hoặc thẩm phân phúc mạc.
5. Cơ chế tác dụng của thuốc :
5.1. Dược lực học:
Mã ATC: J01DD02.
Nhóm dược lý: Kháng sinh nhóm cephalosporin thế hệ 3.
Cơ chế tác dụng:
Ceftazidim ức chế sự sinh tổng hợp thành tế bào vi khuẩn dựa trên sự gắn kết với protein liên kết penicillin. Kêt quả là gián đoạn sinh tông hợp thành tế bào dẫn tới tiêu thành tế bào và làm chết vi khuẩn
Quan hệ dược động học/dược lực học (PK/PD):
Với các cephalosporin, chỉ số dược động học/ dược lực học quan trọng nhất liên quan tới hiệu quả trên in vivo được thây là phân trăm thuốc không gắn kết giữa các khoảng cách liều vẫn duy trì cao hơn nồng độ ức chế tối thiểu (MIC).
Cơ chế kháng thuốc:
Sự kháng kháng sinh của vi khuẩn với ceftazidim có thể do một hoặc các cơ chế sau:
Sự ly giải men beta-lactamase. Ceftazidim có thể bị ly giải bỏi các men beta-lactamase phổ rộng (ESBL), bao gồm SHV và các enzym AmpC có thể làm ức chế hoặc làm yếu đi ở một số loài vi khuẩn Gram (-).
Giảm sự gắn kết của các protein gắn kết penicillin với ceftazidim
Tính không thấm của màng ngoài ngăn sự tiếp cận của ceftazidim với các protein gắn kết penicillin ở các vi khuẩn Gram (-).
Các bơm thụ động ở vi khuấn.
Sự nhạy cảm vỉ sinh vật:
Sự phổ biến kháng thuốc mắc phải có thế khác nhau theo địa lý và thời gian với một số vi khuẩn được lựa chọn và thông tin kháng thuốc theo vùng, đặc biệt khi điều trị các nhiễm trùng nặng. Khi cần thiết, nên tư vấn ý kiến chuyên gia khi mà sự phổ biến kháng thuốc ở địa phương đến mức mà lợi ích của ceftazldim trên một số vi khuẩn vẫn chưa chắc chắn
Các chủng thường là nhay cảm:
Vi khuẩn hiếu khí Gram (+): Streptococcus pyogenes, Streptococcus agalactiae.
Vi khuẩn hiếu khí Gram (-): Citrobacter koseri, Citrobacter koseri, Haemophilus influenzae, Moraxella catarrhalis, Neisseria menigitidis, Pasteurella multocida, Proteus mirabilis, Proteus spp (other), Providencia spp.
Các chủng mà kháng thuốc mắc phải có thế phải cân nhắc
Vi khuẩn hiếu khí gram (-): Acinetobacter baumannii Burkholderia cepacia, Citrobacter freundii, Enterobacter aerogenes, Enterobacter cloacae, Escherichia coli, Klebsiella pneumoniae, Klebsiella spp (other), Pseudomonas aeruginosa, Serratia spp, Morganella morgana.
Vi khuẩn hiếu khí Gram (+): Staphylococcus aureus1, Staphylococcus pneumoniaeLl Viridans group streptococcus
Vi khuẩn kị khí Gram (+): Clostridiumperfringens, Peptostreptococcus spp.
Vi khuẩn kị khí Gram (-): Fusobacterium spp.
Các vi sinh vât kháng thuốc di truyền:
Vi khuân hiếu khí Gram (+): Các chủng Enterococcus spp bao gồm Enterococcus faecalis và Enterococcus faecium. Listeria spp.
Vi khuẩn kị khí Gram (+): Clostridium difficile
Vi khuân kị khí Gram (-): Bacteroides spp. (nhiều chủng Bacteroìdes fragilis kháng thuốc).
Các chủng khác: Chlamydia spp., Mycoplasma spp., Legionella spp
Ghi chú:
(1): S. aureus nhạy cảm với methicillin được xem là có tính nhạy cảm thấp với ceftazidim. Tất cả các loại S. aureus kháng methicillin đều kháng với ceftazidim.
(2): S.pneumoniae đã chứng minh nhạy cảm trung bình hoặc kháng với penicillin có thể dự kiến ít nhất tính nhạy cảm bị giảm với ceftazidim
Tỷ lệ kháng thuốc cao được quan sát ở một hoặc nhiều vùng/quốc gia/khu vực ờ châu Âu.
Cơ chế tác dụng:
Ceftazidim là một kháng sinh cephalosporin thế hệ 3 có tác dụng diệt khuấn do ức chế các enzym tổng hợp thành tế bào vi khuấn.
5.2. Dược động học:
Hấp thu
Sau khi tiêm bắp 500mg hoặc lg ceftazidim, nồng độ đỉnh trong huyết tương nhanh chóng đạt được tương ứng là 18 và 37mg/L. 5 phút sau khi tiêm bolus tĩnh mạch liều 500mg, lg và 2g, nồng độ trong huyết tương tưong ứng là 46, 87 và 170mg/L. Động học của ceftazidim tuyến tính trong khoảng liều đơn là 0.5 -2g theo đưòng tiêm bắp hoặc tĩnh mạch.
Phân bố
Ceftazidim gắn kết với protein huyết tương thấp, khoảng 10%. Nồng độ vượt nồng độ ức chế tối thiểu (MIC) với các tác nhân gây bệnh thường gặp có thể đạt được ở các mô như xương, tim, mật, nước bọt, thủy dịch, hoạt dịch và dịch màng bụng. Ceftazidim dễ dàng đi qua nhau thai và thải trừ qua sữa mẹ. Rất ít đi qua hàng rào máu não còn nguyên vẹn, nồng độ nhỏ ceftazidim trong dịch não tủy (CSF) khi có viêm. Tuy nhiên, khi màng não bị viêm, nồng độ đạt được trong dịch não tủy là 4 – 20 mg/L hoặc nhiều hon.
Chuyển hó
Ceftazidim không bị chuyển hóa.
Thải trừ
Nồng độ sau khi tiêm thuốc giảm với thời gian bán thải là 2 giờ. Ceftazidim được thải trừ qua nước tiểu thông qua lọc cầu thận ở dạng không đổi; khoảng 80 – 90% liều dùng được tái hấp thu từ nước tiểu trong 24 giờ. ít hơn 1% thuốc thải trừ qua mật.
Đối tượng dân số đặc biệt Bênh nhân suy giảm chức năng thân
Thải trừ ceftazidim giảm ở các bệnh nhân suy giảm chức năng thận và nên giảm liều (xem phần Liều dùng và cách dùng).
Bênh nhân suy giảm chức năng gan
Suy giảm chức năng gan nhẹ đến trung bình không ảnh hưỏng đến dược động học của ceftazidim với các cá thê được tiêm tĩnh mạch 2g mỗi 8 giờ trong 5 ngày, miên là chức năng thận vân bình thường (xem phần Liều dùng và cách dùng).
Ngưòi cao tuồi
Thải trừ ceftazidim giảm ỏ’ người cao tuổi chủ yếu do thải trừ ở thận suy giảm theo tuổi. Thời gian bán thải thải trừ trung bình vào khoảng 3,5 – 4 giờ sau với liêu 2g tiêm tĩnh mạch bolus một lân duy nhât hoặc 2 lần/ngày trong 7 ngày ỏ’ bệnh nhân từ 80 tuổi trở lên.
Trẻ em
Thời gian bán thải kéo dài ở trẻ sinh non và sơ sinh từ 4,5 – 7,5 giờ sau các liều từ 25 – 30 mg/kg cân nặng. Tuy nhiên, thời gian bán thải tương đương với người trưởng thành với trẻ từ 2 tháng tuổi
5.3 Giải thích:
Chưa có thông tin. Đang cập nhật.
5.4 Thay thế thuốc :
Chưa có thông tin. Đang cập nhật.
*Lưu ý:
Các thông tin về thuốc trên Pharmog.com chỉ mang tính chất tham khảo – Khi dùng thuốc cần tuyệt đối tuân theo theo hướng dẫn của Bác sĩ
Chúng tôi không chịu trách nhiệm về bất cứ hậu quả nào xảy ra do tự ý dùng thuốc dựa theo các thông tin trên Pharmog.com
6. Phần thông tin kèm theo của thuốc:
6.1. Danh mục tá dược:
Không có
6.2. Tương kỵ :
Với dung dịch natri bicarbonat: Làm giảm tác dụng của thuốc. Không pha ceftazidim vào dung dịch có pH trên 7,5 (không được pha thuốc vào dung dịch natri bicarbonat).
Phối hợp với vancomycin phải tiêm riêng vì gây kết tủa.
Không pha lẫn ceftazidim với các aminoglycosid (gentamicin, streptomycin) hoặc metronidazol. Phải tránh rửa cẩn thận các ống thông và bơm tiêm bằng dung dịch natri clorid 0,9% giữa các lần dùng hai loại thuốc này để tránh gây kết tủa.
6.3. Bảo quản:
Nơi khô, nhiệt độ không quá 300C, tránh ánh sáng.
Dung dịch tiêm bắp (Nồng độ khoảng 250 mg ceftazidim/ml) pha trong nước cất tiêm và dung dịch lidocain hydroclorid 0,5%: Sử dụng trong vòng 18 giờ bảo quản ở nhiệt độ phòng.
Dung dịch tiêm tĩnh mạch (Nồng độ 100 mg ceftazidim/ml hoặc thấp hon) pha trong nước cất tiêm, dung dịch natri clorid 0,9%, dung dịch dextrose 5%: Sử dụng trong vòng 24 giờ bảo quản ở nhiệt độ phòng.
Ceftazidim kém bền vững trong dung dịch natri bicarbonat.
6.4. Thông tin khác :
Dữ liệu an toàn tiền lâm sàng
Dữ liệu tiền lâm sàng cho thấy không có nguy cơ có hại nào với con người dựa trên các nghiên cứu dược lý học an toàn, độc tố liều lặp lại, gây độc với gen, gây độc với sinh sản. Các nghiên cứu trên yêu tô gây ung thư chưa được thực hiện với ceftazidim
6.5 Tài liệu tham khảo:
Dược Thư Quốc Gia Việt Nam


